
Distinguir entre enfermedades que afectan al cerebro no siempre es sencillo. Trastornos como el Alzheimer, el Párkinson o distintos tipos de demencia suelen compartir síntomas, especialmente en sus primeras etapas, lo que complica un diagnóstico certero.
Sin embargo, una investigación reciente liderada por la Universidad de Washington en St. Louis propone una alternativa prometedora: identificar “huellas” proteicas capaces de diferenciar estas patologías con alta precisión.
PUBLICIDAD
El trabajo, publicado en la revista Neuron, se basa en el estudio de proteínas presentes en la sangre y en el líquido cefalorraquídeo —el fluido que rodea y protege tanto el cerebro como la médula espinal—. A partir de este análisis, los científicos lograron reconocer patrones específicos que permiten distinguir entre cuatro enfermedades neurodegenerativas: Alzheimer, Párkinson, demencia con cuerpos de Lewy y demencia frontotemporal.
Qué son las “firmas proteicas” y por qué importan
Para comprender el alcance del hallazgo, es clave entender el concepto de “firma proteica”. Las proteínas son moléculas que cumplen funciones esenciales en el organismo: participan en la comunicación entre células, en la defensa inmunológica y en múltiples procesos biológicos.
PUBLICIDAD
Cuando una enfermedad se desarrolla, ese equilibrio se altera. Algunas proteínas aumentan, otras disminuyen y otras cambian su comportamiento. Ese conjunto de modificaciones forma un patrón identificable, como si fuera una huella digital de la enfermedad.

En este estudio, los investigadores analizaron miles de proteínas en distintos fluidos del cuerpo y utilizaron modelos informáticos avanzados para detectar combinaciones características. Así, lograron reconocer qué patrón corresponde a cada trastorno.
PUBLICIDAD
Uno de los aspectos más relevantes es que muchas de estas señales pueden detectarse en sangre, lo que abre la posibilidad de realizar diagnósticos con un simple análisis, sin necesidad de recurrir a procedimientos más complejos o invasivos.
Diferencias moleculares entre trastornos con síntomas similares
Aunque estas enfermedades pueden parecer similares desde el punto de vista clínico, a nivel molecular presentan diferencias claras. El estudio mostró que cada una tiene su propio perfil proteico, además de compartir ciertos procesos biológicos alterados. Comprender estas diferencias puede ayudar a explicar por qué dos personas con síntomas parecidos pueden, en realidad, estar atravesando trastornos distintos.
PUBLICIDAD
En el caso del Alzheimer, los investigadores identificaron cambios en mecanismos vinculados al sistema inmunológico, la muerte celular programada —un proceso natural mediante el cual el organismo elimina células dañadas— y modificaciones en ciertas moléculas que intervienen en la comunicación celular, fundamentales para el funcionamiento normal del cerebro.
En el Párkinson, en cambio, se observaron proteínas asociadas al estrés celular, es decir, a la forma en que las células responden a condiciones adversas, y a la comunicación entre neuronas.
PUBLICIDAD

La demencia con cuerpos de Lewy presentó alteraciones en rutas relacionadas con factores de crecimiento y con interleucinas, moléculas que cumplen un rol clave en la respuesta inmune y en el mantenimiento de las neuronas.
Por su parte, la demencia frontotemporal mostró cambios en la regulación de la actividad genética de las células nerviosas y en ciertas hormonas, lo que podría estar vinculado al deterioro de regiones del cerebro responsables de la conducta y la toma de decisiones.
PUBLICIDAD
A pesar de estas diferencias, el estudio también encontró procesos compartidos entre las distintas enfermedades, como la inflamación y el deterioro de las sinapsis —los puntos de conexión entre neuronas—, lo que sugiere que existen mecanismos comunes en el daño cerebral.
Diagnóstico más temprano y menos invasivo
Uno de los avances más significativos del trabajo es el desarrollo de modelos predictivos capaces de distinguir entre personas sanas y pacientes, e incluso diferenciar entre distintas enfermedades, utilizando únicamente muestras de sangre o de líquido cefalorraquídeo.
PUBLICIDAD
Según el equipo de la Universidad de Washington en St. Louis, la precisión de estos modelos es comparable a la de métodos tradicionales como los estudios de neuroimagen, que suelen ser más costosos y menos accesibles.

Esto abre la puerta a diagnósticos más tempranos, algo fundamental en enfermedades neurodegenerativas, donde detectar el problema en etapas iniciales puede marcar una gran diferencia en la evolución del paciente.
PUBLICIDAD
Además, permitiría hacer un seguimiento más frecuente de la enfermedad y evaluar la respuesta a tratamientos sin necesidad de recurrir a procedimientos invasivos.
El estudio también destaca que más de la mitad de las proteínas identificadas no habían sido previamente asociadas a estas enfermedades en investigaciones de gran escala. Esto amplía el abanico de posibles biomarcadores, es decir, indicadores biológicos que pueden utilizarse para detectar o monitorear una patología.

Este avance es clave para el desarrollo de la medicina personalizada, un enfoque que busca adaptar los tratamientos a las características específicas de cada paciente. Contar con información detallada sobre los cambios moleculares permitiría diseñar terapias más precisas y efectivas.
Validación internacional y potencial de aplicación clínica
Para garantizar la solidez de los resultados, los investigadores validaron sus hallazgos en múltiples grupos de pacientes de distintas partes del mundo y utilizaron diferentes tecnologías de análisis proteico. También incluyeron participantes con diversas características genéticas, lo que refuerza la aplicabilidad de los resultados.
Además, comprobaron que los patrones detectados se mantienen tanto en sangre como en líquido cefalorraquídeo, lo que aumenta su potencial uso clínico. Sin embargo, los autores señalan que todavía es necesario avanzar en la estandarización de estos métodos antes de que puedan incorporarse de forma rutinaria en la práctica médica.
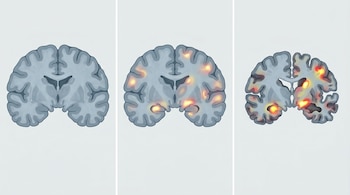
Las enfermedades neurodegenerativas representan uno de los grandes desafíos de la medicina actual, en parte por la dificultad para diagnosticarlas con precisión. Este estudio aporta una herramienta innovadora que podría cambiar ese escenario.
Al demostrar que es posible distinguir entre distintas patologías mediante el análisis de proteínas en fluidos accesibles, la investigación abre el camino hacia diagnósticos más simples, rápidos y menos invasivos.
PUBLICIDAD
PUBLICIDAD
Últimas Noticias
El nuevo antibiótico que abre esperanza para tratar infecciones intrahospitalarias graves
Está dirigido a cuadros severos adquiridos durante la internación, como complicaciones intraabdominales, urinarias y neumonía
Una proteína, dos funciones: cómo el cerebro combina comunicación y defensa
Un estudio de la University of California – Riverside mostró que una molécula puede actuar de manera diferente según el tipo de célula y facilitar la conexión entre neuronas, mientras evita el ingreso de sustancias dañinas
Picazón nocturna y contagio familiar: las claves sobre el oxiuro, el parásito intestinal con más de 10.000 años de historia
El Enterobius vermicularis encuentra su principal foco en espacios de alta concentración infantil y llega al hogar a través de camas, juguetes y corrientes de aire. Cuáles son los síntomas y tratamientos más comunes

Un estudio científico encontró genes de perros golden retrievers asociados a emociones humanas
Investigadores del Reino Unido descubrieron que el comportamiento de esos entrañables perros está vinculado con rasgos psicológicos y cognitivos en las personas. En el Día del Animal, qué implican los resultados

Cómo puede el entorno ruidoso cambiar el ritmo de aprendizaje
Las alertas continuas que produce el bullicio dificultan la atención y fuerzan a reiniciar tareas claves en los niños




