
“Dada la situación actual de la pandemia, la extensión y multiplicidad de los casos, sin que se hubiera logrado, hasta la fecha, una masiva vacunación que permita un control más acelerado de la pandemia (solo un 9% recibió las 2 dosis) y a un aumento de la circulación de nuevas cepas (Manaos, Andina, etc.) sobre las cuales recién se podrá evaluar la eficacia de las vacunas durante los próximos meses, es que creemos que el uso de una droga segura y de bajo costo como la ivermectina, si se comprobara con evidencia firme su efecto beneficioso sobre el tratamiento y la prevención de los casos graves, tendría un impacto fundamental en la evolución de la pandemia”. Este es uno de los párrafos finales de una carta dirigida a la Dra. Carla Vizzoti, Ministra de Salud de la Nación, el pasado 21 de mayo 2021. Junto con la petición, los médicos firmantes (infectólogos, neumólogos y médicos intensivistas, de distintas organizaciones nacionales) presentaron un modelo de protocolo científico con la certeza de que “debe haber un estudio argentino realizado para verificar si sirve o no. El tema es que se usa igual aún sin aprobación, a lo largo y a lo ancho del país”.
Luego de algunas semanas de enviado el protocolo a la Ministra, los responsables de la iniciativa recibieron como toda respuesta un comprobante que decía: “Recibido”.
Nuestro país registra 4.552.750 casos, desde el inicio de la pandemia, y ocupa el puesto número 8 en cantidad de casos a nivel global con 95.521 muertes hasta la fecha. Estos datos son indicativos de la magnitud que ha alcanzado la crisis sanitaria provocada por el virus del SARS-CoV-2. La prolongación en el tiempo de esta pandemia, sumó otro problema: las distintas mutaciones, que llegaron para quedarse, demostrando un mayor poder infeccioso y alta contagiosidad, que eluden el sistema inmune, reduciendo así la efectividad de las vacunas. Es así que se hace evidente la necesidad impostergable de contar con una droga efectiva para combatirlo, situación que aún está pendiente.

Reino Unido lidera la investigación
Además de la carrera por las vacunas –algunos vamos en los últimos puestos- el foco del Estado debiera estar en la financiación de la investigación científica que permitiera poner al alcance de todos un medicamento que cure la enfermedad, o que al menos la atenúe de manera de no llegar a cuadros críticos.
Docenas de grandes ensayos y otros, de menor envergadura, se llevan a cabo en el mundo, con el fin de identificar y acelerar posibles tratamientos anti covid-19. El más importante y representativo es el ensayo RECOVERY, realizado y financiado por Gran Bretaña, iniciado en marzo de 2020, convirtiendo así al Reino Unido en el líder sobre ensayos acerca de un posible tratamiento.

En general, muchos de los tratamientos que se están aplicando no están hechos a medida, sino que son medicamentos ya existentes, utilizados para tratar otras afecciones. En este sentido, y al ser el COVID19 una enfermedad viral, los investigadores han probado con algunos antivirales disponibles en el mercado farmacéutico con resultados alentadores. También se trabaja en la búsqueda de drogas que puedan tratar la enfermedad y frenar la respuesta inmune hiperactiva que aparece en los casos de gravedad. Dicha respuesta es la que causa una serie de complicaciones, como insuficiencia orgánica o sepsis, que llevan a la muerte. Con este fin, los ensayos han evaluado la eficacia de algunos medicamentos antiinflamatorios que detengan la reacción inmunitaria exacerbada.
Fuera de etiqueta
Para el tratamiento de pacientes que ya están internados y bajo advertencia de su utilización fuera de etiqueta (off-label) y solo para emergencias, ya están en uso dos clases de tratamiento.
Según el artículo publicado por The Bmj, el 7 de mayo de 2021, por Chris Baraniuk: “Where are we with drug treatments for covid-19?” (BMJ 2021; 373: n1109 doi:10.1136/bmj. n1109), estos tratamientos involucran sustancias que estimulan o deprimen el sistema inmunitario (inmunomoduladores) como los anticuerpos monoclonales (tocilizumab). Por otro lado, están los corticosteroides (dexametasona o similar) que son medicamentos económicos y de fácil acceso, para tratar los síntomas como la inflamación que produce el virus. La administración de corticoides, en cuanto el paciente ingresa por guardia, reduce la posibilidad de llegar al estado Covid grave, y evita que colapsen las unidades de cuidados intensivos y la demanda de respiradores.
En el caso del tocilizumab (anticuerpo monoclonal) se ha comprobado que ayuda a la respuesta inmunitaria del cuerpo a combatir el virus del SARS- Cov-2 aunque con un precio de mercado muy por encima de la dexametasona. En Gran Bretaña, el Servicio Nacional de Salud, recomienda su uso conjuntamente con la dexametasona para enfermos hospitalizados.
En la siguiente infografía se explica de un modo simple y gráfico las instancias de aplicación y los medicamentos que ya se están utilizando en Inglaterra, en algunos otros países del viejo continente y en Estados Unidos.
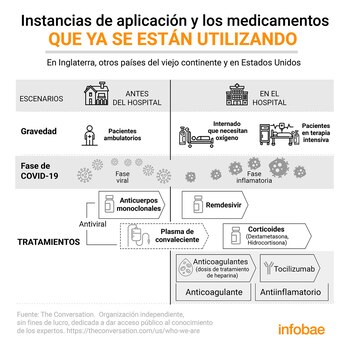
Y en Argentina: ¿qué pasa?
Lo mejor es no enfermarse. Este es el único tratamiento seguro en el país. El resto, son pruebas que se aplican en una u otra clínica, sanatorio u hospital en forma aleatoria, a veces sin ninguna certeza de qué va a funcionar. Los tratamientos de ataque consensuados -al ingreso por guardia- son los corticoides y los anticoagulantes, más la asistencia respiratoria no invasiva como una bigotera o una bolsa de reservorio. Luego de eso, la evolución natural de cada paciente y su respuesta al virus, será lo que determine el futuro de su vida.
Los tratamientos que se han estado aplicando desde el principio de la pandemia son variados, pero ninguno fue protocolizado ni regulado, en su uso y administración.
Remdesivir: según un informe realizado por la Comisión Nacional de Evaluación de Tecnologías de Salud (CONETEC) cuyo equipo de actualización lo integraron: Ariel Izcovich y Fernando Tortosa, supervisado por Manuel Donato, Carlos González Malla y Santiago Torales, con fecha 15 de abril de 2021, “el empleo de remdesivir podría asociarse con beneficios modestos para los pacientes con enfermedad moderada, grave o crítica por COVID-19, sin embargo, la certeza en dichos beneficios es baja. La dificultad para su adquisición en el país y su costo elevado respecto a otras intervenciones, podría afectar la distribución equitativa de la misma y su disponibilidad, en un contexto de alta demanda. En pacientes con enfermedad leve o de reciente comienzo, su eficacia es escasa.”
Tocilizumab: según un informe de Evaluación de Tecnologías Sanitarias COVID N°06, realizado por la Comisión Nacional de Evaluación de Tecnologías de Salud (CONETEC), cuyo equipo de actualización lo integraron: Ariel Izcovich y Fernando Tortosa , supervisado por Manuel Donato, Carlos González Malla y Santiago Torales, con fecha 21 de mayo de 2021, “Tocilizumab se asocia con beneficios sobre desenlaces críticos en pacientes con COVID-19 severo o crítico. Se identificaron potenciales barreras para su uso y el costo comparativo es muy elevado. Las guías de práctica clínica basadas en evidencia relevadas entregan recomendaciones condicionales y discordantes en cuanto a su uso. No existen datos disponibles sobre el efecto de tocilizumab en pacientes con enfermedad leve o moderada. Utilizarlo en una población objetivo más amplia, debido a su elevado costo comparativo, implicaría barreras adicionales. Las guías de práctica clínica basadas en evidencia relevadas, no hacen referencia a este subgrupo de pacientes”.
En este informe aclaran que este medicamento se encuentra aprobado por ANMAT para el tratamiento de enfermedades reumatológicas en adultos y niños y no se encuentra aprobado por ANMAT ni por ninguna otra agencia regulatoria del mundo para el tratamiento de neumonía asociada al COVID-19. Este escenario cambió recientemente cuando la Administración de Medicamentos y Alimentos (FDA), agencia del Gobierno de los Estados Unidos autorizó el pasado 24 de junio el uso de tocilizumab para pacientes hospitalizados adultos y niños a partir de los 2 años de edad .
En Argentina, el precio de venta al público de un frasco ampolla de tocilizumab de 200mg/10ml es de ARS 56.930, mientras que para el de 400mg/20ml es de ARS 113.861 (31/03/2021). Con estos precios el costo del tratamiento con 600 mg sería de ARS 170.791 (USD 1.833) y para el de 800 mg sería de ARS 227.722 (USD 2.445).
Ivermectina. Las conclusiones que se desprenden del informe realizado por Ariel Izcovich y Fernando Tortosa, supervisado por Manuel Donato, Carlos González Malla y Santiago Torales, con fecha 7 de mayo de 2021, explican que “En personas no infectadas, expuestas al SARS-CoV-2, existe incertidumbre en el efecto de la ivermectina para prevenir la infección sintomática, presunta o confirmada por este virus. El cuerpo de evidencia disponible hasta el momento muestra que, en pacientes con COVID-19, existe incertidumbre en el efecto de ivermectina sobre la mortalidad y los eventos adversos graves. La ivermectina podría no tener efecto sobre el ingreso en ventilación mecánica o la duración de la internación y probablemente no tenga efecto en el tiempo de resolución de los síntomas.”
A pesar de estas supuestas “barreras para su implementación y uso ”la ivermectina se encuentra ampliamente disponible en Argentina y está aprobada por ANMAT para el tratamiento de infecciones parasitarias, no así para su uso en la prevención de la infección por el virus SARS-CoV-2 o para el tratamiento de personas con COVID-19. Una ventaja es su bajo costo y fácil acceso y disponibilidad en el mercado de medicamentos.
Suero equino. Aprobado en diciembre del 2020 por la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT). La Comisión Nacional de Evaluación de Tecnologías de Salud (CONETEC), en un informe con fecha 21 de abril de 2021, concluye: “El cuerpo de evidencia disponible hasta el momento muestra que existe incertidumbre en el efecto de los anticuerpos policlonales equinos sobre la mortalidad y el ingreso en ventilación mecánica. (…) La incertidumbre sobre el efecto de la tecnología evaluada sobre los desenlaces críticos para pacientes hospitalizados con COVI-19 (mortalidad y requerimiento de ventilación invasiva) determina que la certeza en los efectos de suero equino sobre la salud de pacientes con COVID-19 sea muy baja. A pesar que la tecnología se produce en Argentina lo que facilitaría su acceso, encontramos barreras relacionadas con una amplia población objetivo y elevado costo comparativo de esta intervención que podrían acarrear problemas de producción y afectar la distribución equitativa en situaciones de alta demanda”. Sin embargo, el suero “CoviFab” producido por un grupo de científicos argentinos, de la Universidad Nacional de San Martin (UNSAM), demostró reducir hasta en un 45% la mortalidad de los infectados, en un 24% la necesidad de recurrir a terapia intensiva y un 36% el requerimiento de respirador, en pacientes con enfermedad moderada a severa. Y el dato curioso al respecto es que, hace pocas semanas, según aseguraron fuentes expertas, el fabricante de este tratamiento manifestó su preocupación por el vencimiento de las ampollas que nadie usa.
Plasma de convalecientes. La Secretaría de Calidad en Salud, del Ministerio de Salud de la Nación, publicó en el Boletín Oficial, con fecha 29 de enero 2021, el consenso para el uso del plasma con fines terapéuticos. La principal condición para su administración es que deben recibirlo solo los enfermos con menos de 3 días de iniciados los síntomas, que no presenten criterios de gravedad. Actualmente existe muy baja o nula utilización de plasma en los centros sanitarios por varias razones: ¿la principal? la falta de una campaña pública de donación, lo cual reduce la existencia de bancos de plasma que puedan cubrir una posible demanda. Y otra: muchos hospitales y clínicas han desestimado su uso.
SEGUIR LEYENDO:
Últimas Noticias
La empresa en un mundo sin nosotros
Un reciente anuncio propone modificar la legislación para permitir entidades jurídicas gestionadas por sistemas autónomos, lo que plantea desafíos regulatorios y podría transformar el equilibrio en el ámbito del trabajo, la tributación y la responsabilidad civil

“El poder tributario es del pueblo”
Un proyecto de ley avanza en el Congreso para restituir el control parlamentario sobre el ISC. La propuesta busca que los cambios en la tasa solo puedan realizarse mediante leyes aprobadas por el Legislativo o por delegación expresa, garantizando mayor control de la potestad tributaria

Fianza arrendaticia en Perú: entre la protección y la desconfianza
Una demanda que el sistema no logra interpretar

La nueva frontera de la IA no está en internet, está en los objetos
Los sistemas inteligentes comienzan a interactuar con objetos, laboratorios y dispositivos, abriendo una nueva etapa orientada a la manipulación del entorno más allá de la información digital y las pantallas tradicionales

70 años de educación privada universitaria en Argentina
La Universidad del Salvador, la Universidad Católica de Córdoba y la Universidad del Museo Social Argentino fueron pioneras del sistema universitario privado argentino


