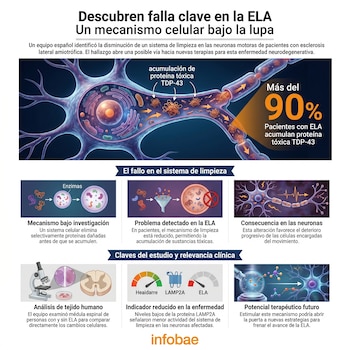
La esclerosis lateral amiotrófica (ELA) es una enfermedad del sistema nervioso que provoca un deterioro progresivo del cuerpo. Su progresión es rápida, afecta la capacidad de movimiento y, en la mayoría de los casos, no cuenta con tratamientos capaces de frenar su avance.
En este contexto, un equipo de científicos españoles dio un paso relevante al identificar un fallo específico dentro de las células nerviosas que podría explicar parte del daño que produce la enfermedad.
PUBLICIDAD
La ELA es considerada una patología poco frecuente. Según la Organización Mundial de la Salud (OMS), su prevalencia se ubica en torno a entre 3 y 8 casos por cada 100.000 habitantes, lo que refuerza el desafío que implica investigarla y desarrollar tratamientos efectivos.

El hallazgo, publicado en la revista Neuropathologica Communications, apunta a un sistema interno que funciona como un mecanismo de limpieza. Cuando este proceso falla, las células del cerebro —llamadas neuronas— comienzan a acumular sustancias defectuosas que terminan siendo tóxicas. Con el tiempo, esa acumulación contribuye al deterioro característico de la enfermedad.
PUBLICIDAD
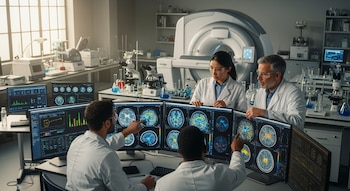
El trabajo fue liderado por investigadores del Instituto de Neurociencias de la Universidad Miguel Hernández de Elche y se basó en el análisis directo de tejido humano, lo que refuerza la relevancia de los resultados desde el punto de vista clínico.
Importancia del sistema de limpieza celular en las neuronas motoras
Para entender la importancia del descubrimiento, primero hay que mirar qué ocurre dentro de las células. En su interior, las proteínas cumplen funciones fundamentales, pero también pueden dañarse o dejar de funcionar correctamente. Cuando eso ocurre, el organismo cuenta con mecanismos para eliminarlas y evitar que generen problemas.
PUBLICIDAD
Uno de esos sistemas es la autofagia mediada por chaperonas. Aunque el nombre es técnico, su función es clara: actúa como un “control de calidad” que identifica proteínas dañadas y las elimina de forma selectiva, es decir, reconoce específicamente qué debe eliminarse.
Este mecanismo es especialmente importante en las neuronas motoras, las células encargadas de enviar las órdenes del cerebro a los músculos. Gracias a ellas podemos realizar acciones como caminar, hablar o respirar.
PUBLICIDAD
Cuando estas células se deterioran, los músculos dejan de recibir señales y comienzan a debilitarse. Con el tiempo, el cuerpo pierde funciones básicas, lo que explica los síntomas progresivos de la ELA.
Qué ocurre en la ELA: acumulación de proteínas tóxicas
En la ELA, uno de los rasgos más conocidos es la acumulación anormal de una proteína llamada TDP-43. En condiciones normales, cumple funciones dentro de la célula, pero cuando se altera, forma agregados que resultan perjudiciales.
PUBLICIDAD
Más del 90% de los pacientes presentan esta acumulación, lo que la convierte en una de las principales señales de la enfermedad. Sin embargo, hasta ahora no estaba completamente claro por qué se produce ni qué mecanismos fallan para evitarla.

El nuevo estudio aporta una pieza clave a ese rompecabezas. Los investigadores comprobaron que el sistema de autofagia mediada por chaperonas está disminuido en las neuronas de personas con ELA. En otras palabras, el “sistema de limpieza” no funciona como debería, lo que permite que las proteínas defectuosas se acumulen.
PUBLICIDAD
Cómo se realizó el estudio
Para llegar a estas conclusiones, los científicos analizaron muestras de médula espinal donadas por personas con ELA y por individuos sin la enfermedad. Este enfoque permitió comparar directamente qué ocurre en ambos casos.
Utilizaron técnicas avanzadas, como inmunohistoquímica e inmunofluorescencia, que permiten visualizar y medir proteínas dentro de las células. En particular, se enfocaron en una proteína llamada LAMP2A, que actúa como indicador de la actividad del sistema de limpieza celular.
PUBLICIDAD
Los resultados fueron claros: en las neuronas sanas, los niveles de LAMP2A eran elevados, lo que indica una actividad intensa del mecanismo de eliminación de proteínas. En cambio, en las neuronas de pacientes con ELA, esos niveles estaban significativamente reducidos.
Esta diferencia sugiere que las células afectadas pierden capacidad para eliminar residuos dañinos, lo que contribuye a su deterioro.
PUBLICIDAD
Un factor central en la degeneración
El estudio también mostró que las neuronas motoras dependen especialmente de este sistema para sobrevivir. A diferencia de otros tipos celulares, necesitan niveles muy altos de actividad de este mecanismo para mantenerse en buen estado.
Cuando esa actividad disminuye, las primeras células en verse afectadas son justamente las relacionadas con el movimiento. Esto coincide con los síntomas iniciales de la ELA, que suelen incluir debilidad muscular y pérdida progresiva de la movilidad.
El profesor Salvador Martínez, responsable del laboratorio que lideró la investigación, destacó que identificar procesos celulares directamente vinculados con la supervivencia neuronal resulta fundamental para avanzar en el desarrollo de tratamientos.
Una posible puerta hacia nuevas terapias
Uno de los aspectos más prometedores del hallazgo es su potencial aplicación clínica. Si la disminución de este sistema contribuye al avance de la enfermedad, entonces estimularlo podría convertirse en una estrategia terapéutica.
En términos simples, la idea sería “reactivar” o potenciar el mecanismo de limpieza celular para ayudar a las neuronas a eliminar proteínas dañinas antes de que causen daño irreversible. Aunque esta línea de trabajo aún se encuentra en etapas iniciales, abre una posibilidad concreta en un campo donde las opciones terapéuticas son limitadas.

Otro punto destacado del estudio es el uso de muestras humanas. Muchos trabajos en neurociencia se realizan en modelos animales o celulares, lo que puede dificultar la extrapolación de resultados a pacientes.
En este caso, el análisis directo de tejido humano permite observar el fenómeno tal como ocurre en la enfermedad real, lo que aumenta la validez de las conclusiones.
Un paso más en la comprensión de la ELA
La ELA continúa siendo una enfermedad con causas en gran parte desconocidas. Su evolución suele conducir, en pocos años, a la pérdida de funciones vitales como la respiración. Frente a este panorama, cada avance en la comprensión de sus mecanismos resulta valioso.
La identificación de un sistema celular defectuoso aporta una nueva perspectiva sobre cómo se origina el daño neuronal. Más importante aún, ofrece un punto de partida concreto para el desarrollo de futuras terapias.
Aunque todavía no existe una cura, este hallazgo aporta una nueva pista para entender qué ocurre en la ELA y hacia dónde podrían orientarse futuras investigaciones.
PUBLICIDAD
PUBLICIDAD
Últimas Noticias
Un tipo de narcolepsia podría estar relacionado con una respuesta del sistema inmune, afirma un estudio
Durante más de veinte años, la ciencia atribuyó este trastorno a una sola zona cerebral, pero investigadores de la University of California identificaron una segunda región afectada que cambia la comprensión de la enfermedad

Un método con IA revela datos inéditos sobre el ADN humano y abre nuevas vías para tratar enfermedades
Un equipo internacional logró mapear la estructura interna de los nucleosomas y detectar 14 estados diferentes, lo que podría transformar la comprensión y el abordaje de múltiples patologías

Qué es la cardiopatía isquémica, el diagnóstico por el que fue operado Diego Peretti
El actor fue sometido a una intervención en Buenos Aires tras detectarse una obstrucción en sus arterias coronarias, una condición que afecta a millones de personas y requiere atención médica especializada
La sal eleva la presión arterial y provoca el envejecimiento prematuro de las células arteriales, afirma un estudio
Una investigación realizada en modelos animales por la Universidad del Sur de Alabama identificó que el sodio activa la interleucina-16, una proteína inflamatoria que deteriora la función de los vasos sanguíneos

Una vacuna experimental contra el VIH logró neutralizar el 49% de las variantes del virus en modelos animales: cómo funciona
El equipo del Karolinska Institutet ya trabaja en adaptar la estrategia para ensayos en humanos, con el objetivo de optimizar los inmunógenos y los esquemas de administración frente a la gran diversidad genética del virus