
Un equipo internacional presentó el primer atlas genético del hígado humano con resolución celular, desarrollado por el Weizmann Institute of Science junto al Sheba Medical Center y la Mayo Clinic. El trabajo revela una organización interna dividida en ocho zonas funcionales, superando el modelo tradicional de tres áreas principales, y ofrece nuevos caminos para comprender y tratar enfermedades hepáticas frecuentes.
Este nuevo atlas mapea en detalle las funciones y la distribución espacial de miles de genes en células hepáticas sanas, gracias al análisis de muestras obtenidas de ocho donantes vivos.
PUBLICIDAD
El recurso permite identificar cómo se asignan más de 500 tareas metabólicas al interior del órgano, por qué ciertas áreas son más vulnerables a trastornos como la enfermedad hepática grasa y cómo las diferencias con otros mamíferos podrían respaldar el futuro desarrollo de terapias dirigidas para afecciones concretas.
El estudio, publicado en Nature, fue coordinado por el grupo del Prof. Shalev Itzkovitz del Weizmann Institute of Science, empleando tecnologías avanzadas para mapear de manera individual la expresión genética en las células hepáticas.
PUBLICIDAD
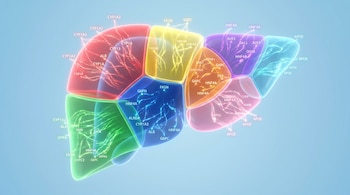
Este enfoque resolvió la dificultad histórica de cartografiar la función interna del hígado por la escasez de muestras sanas y permitió describir ocho zonas funcionales del órgano, cada una con funciones específicas. Así, se cuestiona el modelo clásico de tres áreas principales aceptado durante décadas.
Itzkovitz destacó la relevancia del hallazgo: “Miles de genes muestran actividad distinta según la ubicación de la célula en el hígado, lo que apunta a una organización interna mucho más precisa y compleja que lo pensado”.
PUBLICIDAD
El mapa del lóbulo hepático humano y las diferentes vulnerabilidades
La precisión del atlas permite comprender cómo el hígado mantiene múltiples funciones vitales a la vez. Ahora cualquier laboratorio puede investigar por qué algunas zonas son más propensas a enfermedades metabólicas, inflamatorias o tumorales.
Cada zona cumple funciones distintas, por eso no todas se enferman de la misma manera. Por ejemplo, los problemas metabólicos —como la acumulación de grasa— suelen aparecer en la parte central, mientras que las inflamaciones causadas por virus o por el propio sistema inmunológico son más frecuentes en las áreas externas.
PUBLICIDAD

El cáncer de hígado y las metástasis también exhiben preferencias espaciales, lo que subraya la importancia de la organización interna identificada: ciertas regiones, por su especialización celular y flujo sanguíneo, concentran procesos metabólicos o defensivos que las vuelven más o menos susceptibles a distintos padecimientos.
Diferencias entre el hígado humano y el de otros mamíferos
El equipo del Weizmann Institute of Science comparó el hígado humano con el de ratones, cerdos y vacas para detectar singularidades.
En todos los mamíferos, la sangre circula desde las zonas externas hacia el centro, transportando oxígeno y nutrientes. Sin embargo, en humanos esa parte central sigue funcionando de manera muy activa incluso cuando los recursos son bajos. En esa región, las células realizan tareas esenciales, como producir energía cuando no hay alimento, fabricar grasas y eliminar sustancias tóxicas.
PUBLICIDAD
Una diferencia importante está en dónde se almacena la glucosa, que es una de las principales fuentes de energía del cuerpo. En los ratones, ocurre en las zonas externas, mientras que en humanos se concentra en el centro. Esto permite un acceso más rápido y una liberación más controlada de energía según lo que el organismo necesita.
Los especialistas señalan que esta “división del trabajo” facilita el almacenamiento eficiente de hidratos de carbono: las células centrales absorben y almacenan glucosa, mientras las periféricas transforman lactato en glucosa para reforzar las reservas durante el ayuno.
PUBLICIDAD
Sin embargo, el sistema no está adaptado a dietas actuales ricas en grasas y azúcares, lo que contribuye a la acumulación de grasa en el hígado y a la fibrosis.
El estudio también identificó un patrón único en la ubicación de las células de Kupffer—encargadas de defensas inmunitarias y de remover células dañadas. El Dr. Oran Yakubovsky explicó que, en humanos, estas células se concentran en el centro del lóbulo, posiblemente como respuesta al mayor desgaste celular en esa zona, a diferencia de otros mamíferos, en los que se localizan en la periferia.
PUBLICIDAD
Implicancias clínicas y nuevos caminos de tratamiento
En una etapa posterior, los investigadores del Weizmann Institute of Science analizaron las implicaciones clínicas del atlas. Se centraron en la enfermedad hepática grasa relacionada con disfunción metabólica, una patología frecuente asociada a obesidad y diabetes.
Al comparar hepatocitos (células principales del hígado) sanos y afectados, observaron una respuesta protectora: las células suprimen los genes encargados de incorporar y fabricar grasa, y activan aquellos responsables de su descomposición.
PUBLICIDAD
Identificaron una limitación: al acumular grasa, disminuye la producción de elementos de la mitocondria que descomponen los lípidos. Esto merma la capacidad defensiva del hígado contra el exceso de grasa y eleva el riesgo de daño e inflamación persistente.
El atlas muestra que no todas las zonas se enferman de la misma manera. Algunos problemas, como los metabólicos, las inflamaciones o el cáncer, tienden a aparecer en áreas específicas. Esto ocurre porque cada región tiene funciones y características propias, lo que la hace más vulnerable a ciertos trastornos que a otros.
Aplicaciones futuras del atlas genético del hígado
La creación de este nuevo atlas asienta una base para diseñar terapias dirigidas a genes específicos en las regiones más vulnerables del hígado. Según el Weizmann Institute of Science, la metodología basada en análisis de donantes vivos puede trasladarse al estudio de otros órganos humanos aún no cartografiados con esta precisión.
Esta cartografía ultradetallada podría transformar el modo en que la ciencia comprende y trata no solo las enfermedades hepáticas, sino también otros padecimientos vinculados a la estructura interna de órganos y tejidos. La capacidad de intervenir de forma precisa en áreas particulares abrirá nuevas posibilidades en la investigación biomédica en el futuro próximo.
A partir de este avance, el Weizmann Institute of Science considera que es posible iniciar una nueva era en la medicina personalizada, aplicando métodos similares para descifrar la estructura y función de órganos que hasta hoy permanecen inexplorados con tal resolución.
PUBLICIDAD
PUBLICIDAD
Últimas Noticias
Cuáles son los ejercicios ideales para aliviar el dolor de ciática y cuándo consultar al médico
Los estiramientos lentos y progresivos contribuyen a reducir las molestias y previenen nuevos episodios sin sobrecargar la zona lumbar

La primera terapia genética para rejuvenecer células humanas inicia pruebas en pacientes con glaucoma
El avance, destacado por el especialista en longevidad Eric Topol, marca el inicio de un ensayo en Estados Unidos donde se busca revertir el envejecimiento celular activando genes en personas con glaucoma avanzado

Una encuesta regional expone retrasos y obstáculos en la atención de enfermedades autoinmunes de la piel
El relevamiento realizado en 14 países, presentado en la Reunión Anual de Dermatólogos Latinoamericanos, halló demoras diagnósticas de hasta 10 años, discontinuidad terapéutica, y fuerte impacto emocional y social

Cómo los horarios irregulares de sueño pueden afectar la memoria y el lenguaje infantil
La investigación muestra que la constancia en las rutinas diarias impacta la adquisición de palabras y la retención de información visual, incluso si se cumplen las horas recomendadas para descansar

Las mujeres con menopausia temprana tienen mayor riesgo de padecer ACV o infarto, según un estudio
Una investigación publicada en The Lancet Obstetrics, Gynaecology, & Women’s Health analizó a más de 100 mil mujeres con inicio del climaterio antes de los 45 años. Cuál es la causa



