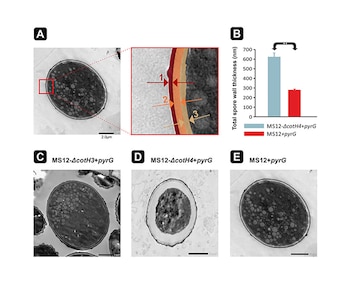
El hallazgo de nuevos genes clave en la virulencia de hongos representa un avance para comprender y combatir infecciones graves. Un estudio del equipo de la Universidad de Murcia (UMU), junto al Centro de Investigaciones Biológicas Margarita Salas (CSIC), identificó los genes dkl y dfl como controladores de la transición entre los estados de levadura y micelio en hongos del orden Mucorales.
Este proceso es esencial para la capacidad de estos hongos de infectar a humanos y provocar enfermedades como la mucormicosis, ya que los genes dkl y dfl funcionan como interruptores que regulan tanto la forma patógena del hongo como su adaptación al entorno.
Según los investigadores, manipular estos genes podría ser determinante para limitar o bloquear el desarrollo de infecciones fúngicas graves. La investigación se centró en el hongo Mucor lusitanicus, considerado modelo experimental para el estudio de la patogenicidad en Mucorales. El estudio fue publicado en la revista científica Current Biology y difundido por la revista Muy Interesante.
Qué son y cómo se comportan estos hongos
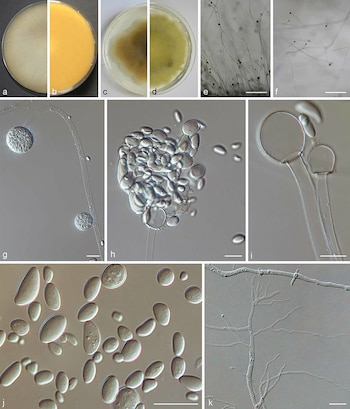
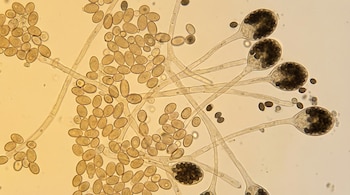
Los hongos del orden Mucorales destacan por su capacidad de adaptarse a múltiples entornos y por ser patógenos relevantes en humanos, especialmente en personas inmunodeprimidas. Estos organismos, responsables de la mucormicosis, muestran flexibilidad alternando entre las formas de levadura y micelio según las condiciones ambientales.
Esta plasticidad morfológica les permite sobrevivir tanto en suelos como en organismos vivos. Para comprender los mecanismos de adaptación y virulencia, los investigadores eligieron Mucor lusitanicus como modelo de estudio, ya que comparte los rasgos esenciales de los Mucorales y facilita el análisis genético y morfológico.
Estructuras y duplicación: así se adaptan

El artículo describe que los genes dkl y dfl se originaron por duplicación genética dentro de los Mucorales.
Este fenómeno permitió que ambos genes coexistan en el genoma, ubicados en una estructura particular denominada head-to-head, donde sus secuencias se disponen de forma opuesta y comparten regiones reguladoras.
Esta singular disposición favorece una regulación coordinada, lo que permite a los hongos responder rápidamente a los cambios del entorno. Según el análisis, la duplicación y el arreglo head-to-head representan una estrategia evolutiva que incrementa la capacidad adaptativa y la virulencia del hongo, diferenciándolo de otros grupos fúngicos.
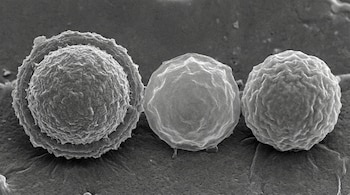
La transición morfológica reversible entre levadura y micelio resulta fundamental en la virulencia de los Mucorales.
El estudio revela que la forma de levadura predomina en entornos anaeróbicos, como los tejidos humanos infectados, mientras que el hongo adopta la forma de micelio en ambientes con mayor presencia de oxígeno.
Esta reversibilidad dota al patógeno de flexibilidad y le permite colonizar diferentes nichos en el huésped, aumentando su capacidad de causar mucormicosis. La coordinación de este cambio está a cargo de los genes dkl y dfl, que activan o desactivan diversas rutas genéticas según las condiciones ambientales.
Claves del avance y nuevas ventanas terapéuticas
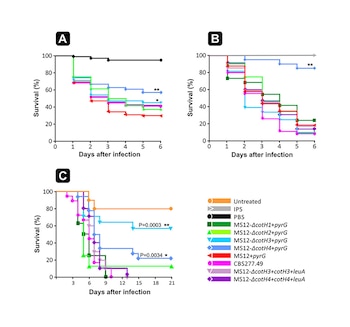
El trabajo publicado en Current Biology sugiere que los mecanismos regulados por los genes dkl y dfl podrían ser el blanco de futuros tratamientos antifúngicos.
Estos genes y su estructura head-to-head son exclusivos de los Mucorales, lo que permitiría diseñar medicamentos que los inhiban de manera selectiva y sin afectar a la microbiota beneficiosa o a otros organismos.
La especificidad terapéutica que se plantea abre la posibilidad de tratamientos más eficazes y con menos efectos secundarios para combatir la mucormicosis y otras infecciones fúngicas severas.
La investigación destaca que la presencia de mecanismos similares en diferentes linajes de hongos patógenos constituye un caso de convergencia evolutiva.
Aunque Mucorales y otros grupos fúngicos han generado rutas genéticas distintas, el efecto es comparable: todos adquieren la capacidad de alternar entre formas morfológicas para sobrevivir y adaptarse en el huésped.
El que múltiples linajes converjan en esta solución indica que el cambio de forma representa una ventaja adaptativa recurrente en la evolución de los hongos patógenos y explica por qué la patogenicidad ha aparecido varias veces de manera independiente.
Limitaciones actuales y futuros fármacos
A pesar de los avances, la revista Muy Interesante advierte que trasladar estos descubrimientos a la clínica conlleva desafíos científicos y técnicos.
Comprender en detalle cómo los genes dkl y dfl interactúan con el resto de procesos celulares requiere estudios adicionales. Los futuros antifúngicos obligatoriamente deben ser altamente específicos para evitar daños a células humanas o microorganismos beneficiosos, dificultad que aún está lejos de resolverse.
También resulta complicado lograr que los fármacos penetren en los tejidos más profundos afectados por la mucormicosis, enfermedad que suele invadir áreas de difícil acceso. Además, la resistencia natural de los Mucorales a los tratamientos actuales obliga a diseñar soluciones innovadoras, y la escasez de modelos animales adecuados dificulta la validación de nuevos compuestos. Todos estos factores presentan obstáculos para el desarrollo de terapias basadas en estos hallazgos.
Últimas Noticias
La realidad virtual puede inducir emociones positivas y bienestar psicológico, según un estudio internacional
Un análisis de 122 estudios muestra que la geometría, la iluminación y los colores influyen directamente en la generación de estados de calma y alegría en usuarios de estas tecnologías

Descubren una nueva enfermedad genética rara que produciría trastornos graves en el desarrollo
El hallazgo de RPN1-CDG, publicado en Human Genetics and Genomics Advances, permite poner nombre a una condición poco frecuente y brinda nuevos diagnósticos a pacientes con síntomas complejos
Cuál es el vínculo entre el consumo de ultraprocesados y la acumulación de grasa muscular
Científicos de los Estados Unidos hicieron un análisis de 615 personas, con una dieta compuesta en promedio por un 41% de alimentos industrializados. Qué encontraron

Por qué algunas lesiones medulares pueden afectar el equilibrio y la forma de caminar
Un estudio identificó patrones anómalos en la señal nerviosa en personas con esta condición de manera incompleta, que explican la inestabilidad durante la marcha. El hallazgo abre la puerta a terapias más personalizadas
Los consejos de la NASA para dormir bien y lograr un sueño reparador
La agencia espacial desarrolló estrategias para que los astronautas logren un descanso óptimo en la ingravidez del espacio, y sus recomendaciones pueden aplicarse en la Tierra. La experiencia de los tripulantes de Artemis II



