
La enfermedad de Alzheimer sigue siendo uno de los mayores desafíos de la medicina moderna. A pesar de décadas de investigación, aún no existe una cura capaz de detener su progresión. Sin embargo, un nuevo estudio realizado por investigadores de la Mayo Clinic aporta pistas importantes sobre los mecanismos que podrían estar detrás del deterioro cerebral.
Según la Organización Mundial de la Salud (OMS), alrededor de 57 millones de personas viven con demencia en el mundo, y la enfermedad de Alzheimer representa entre el 60% y el 70% de los casos.
Se trata de una enfermedad progresiva que deteriora la memoria, el pensamiento y la capacidad para realizar actividades cotidianas, afectando profundamente la autonomía de quienes la padecen y generando un fuerte impacto en las familias y los sistemas de salud.

En ese contexto, el nuevo trabajo identificó cambios epigenéticos significativos en el ADN de cerebros afectados por Alzheimer, especialmente en células llamadas oligodendrocitos. Estas modificaciones no alteran la secuencia genética, pero sí influyen en cómo se activan o desactivan determinados genes, lo que puede afectar el funcionamiento celular.
Los resultados ayudan a explicar por qué la enfermedad evoluciona de manera diferente en cada persona y señalan posibles rutas moleculares que podrían aprovecharse para desarrollar tratamientos más específicos en el futuro.
Qué son los cambios epigenéticos y por qué importan
Para entender la importancia del hallazgo, primero es necesario explicar el concepto de epigenética. Aunque todas las células del cuerpo contienen el mismo ADN, no todas utilizan la misma información genética. Las marcas epigenéticas funcionan como un sistema de regulación que determina qué genes se activan y cuáles permanecen inactivos.
Para entenderlo mejor, es como si el ADN fuera un libro con miles de páginas, la epigenética actuaría como un sistema de marcadores que indica qué capítulos deben leerse en cada momento.
Cuando estas señales químicas cambian, también puede modificarse el comportamiento de las células. En el caso del Alzheimer, esas alteraciones podrían influir en la forma en que el cerebro responde al daño y en la velocidad con la que avanza la enfermedad.
Cómo se analizó el ADN en cerebros con Alzheimer
El equipo liderado por la doctora Nilüfer Ertekin-Taner, especialista en neurogenética de Mayo Clinic, analizó tejido cerebral proveniente del Banco de Cerebros del Departamento de Neurociencias de la institución.
Los investigadores estudiaron muestras de 472 personas con Alzheimer, enfocándose en un tipo específico de marca epigenética: la metilación del ADN, un proceso químico que regula la expresión de los genes.

Además de examinar estas modificaciones, el equipo comparó los resultados con niveles de proteínas asociadas a la enfermedad y con observaciones microscópicas del tejido cerebral. Los hallazgos también fueron contrastados con conjuntos de datos independientes para reforzar su validez.
El rol de los oligodendrocitos y la mielina
Uno de los resultados más relevantes fue que muchas de las alteraciones epigenéticas identificadas se concentraban en los oligodendrocitos.
Estas células cumplen una función esencial en el sistema nervioso: producen mielina, una sustancia que recubre las fibras nerviosas y permite que los impulsos eléctricos viajen con mayor rapidez entre neuronas.
Puede pensarse en la mielina como el aislamiento de un cable eléctrico. Cuando ese recubrimiento se deteriora, las señales nerviosas se transmiten con menos eficiencia.
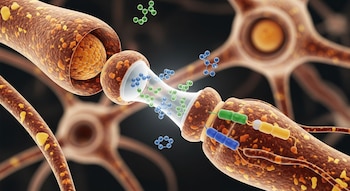
Los hallazgos sugieren que los problemas en los oligodendrocitos y en la producción de mielina podrían desempeñar un papel más importante en el Alzheimer de lo que se creía hasta ahora.
La conexión con la proteína tau
El estudio también encontró una fuerte relación entre las modificaciones epigenéticas detectadas y la presencia de proteína tau, una de las moléculas más vinculadas con el Alzheimer.
En esta enfermedad, la tau forma estructuras anormales conocidas como ovillos neurofibrilares, que interfieren con el funcionamiento de las neuronas y contribuyen al deterioro cognitivo.
Los investigadores observaron que gran parte de las alteraciones epigenéticas analizadas estaban asociadas a la acumulación de esta proteína, lo que sugiere una interacción entre ambos procesos biológicos.
Según explicó Ertekin-Taner, estos resultados refuerzan la idea de que la alteración de oligodendrocitos y mielina podría ser un componente central del desarrollo de la enfermedad.
Entre los genes que mostraron cambios relevantes aparece LDB3, cuya función en el contexto del Alzheimer aún comienza a investigarse.
El interés de los científicos radica en que los cambios epigenéticos, a diferencia de las mutaciones genéticas, pueden ser potencialmente reversibles. Esto abre la posibilidad de desarrollar tratamientos capaces de modificar la expresión genética o de proteger el funcionamiento de los oligodendrocitos.
Aunque estas estrategias aún se encuentran en etapas iniciales, representan una vía prometedora para futuras terapias.
Un atlas digital para impulsar la investigación
Con el objetivo de acelerar los avances científicos, el equipo también desarrolló una herramienta digital abierta llamada Multiomic Atlas of AD Brain Endophenotypes.
Esta plataforma permite a investigadores de todo el mundo explorar los datos generados por el estudio, buscar genes específicos y analizar sus asociaciones con distintos procesos biológicos relacionados con el Alzheimer.

La doctora Stephanie Oatman, autora principal del trabajo, explicó el propósito de esta iniciativa: “Facilitar el acceso a los análisis realizados puede impulsar el trabajo de otros equipos y, a futuro, beneficiar a los pacientes”.
El atlas ofrece búsquedas por nombre de gen o ubicación cromosómica y presenta los resultados mediante tablas e imágenes interactivas.
Un paso más para comprender el Alzheimer
Comprender las alteraciones moleculares que ocurren en el cerebro es fundamental para avanzar hacia tratamientos más eficaces contra la demencia.
El nuevo estudio sugiere que la epigenética —y en particular los cambios que afectan a oligodendrocitos y mielina— podría desempeñar un papel más importante de lo que se pensaba en el desarrollo del Alzheimer.
Aunque aún queda mucho por investigar, estos hallazgos ofrecen una nueva perspectiva sobre cómo progresa la enfermedad y abren la puerta a estrategias terapéuticas que busquen modificar las rutas biológicas que la impulsan.
Últimas Noticias
Descubren cómo un tipo de hantavirus de Sudamérica ingresa a las células humanas
El patógeno puede transmitirse a partir de roedores y de otras personas afectadas. Fue estudiado por investigadores de los Estados Unidos. Cómo fue el primer paso hacia una vacuna

El sueño profundo rompe la sincronía entre la respiración y la actividad cerebral, afirma un estudio
Un avance experimental en modelos animales revela que la desconexión entre ambos procesos ocurre especialmente durante las ondas delta, mientras que en la vigilia y bajo anestesia se mantiene la coordinación

Obesidad: por qué el reto no es solo bajar de peso y cuáles son las claves para lograr resultados duraderos
Especialistas advierten que las estrategias más efectivas incluyen acompañamiento profesional, educación nutricional y otras herramientas para preservar la salud metabólica

Día Mundial de VPH: el virus del papiloma humano puede afectar al 80% de la población
La identificación precoz de infecciones persistentes por genotipos de alto riesgo es clave. Los últimos avances presentados en 27° Congreso Europeo de Oncología Ginecológica

¿Despertarse a las 5 AM es bueno para la salud? Qué dicen los expertos en sueño
Especialistas advierten que forzar el despertar temprano puede afectar el ánimo, el rendimiento y el bienestar. Subrayan la necesidad de respetar el cronotipo individual y mantener una rutina regular para favorecer un descanso adecuado




