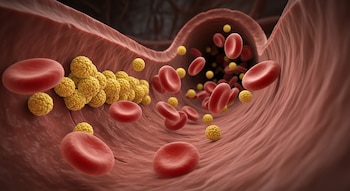
La hipercolesterolemia familiar (HF) es una enfermedad hereditaria que se manifiesta desde el nacimiento y provoca un aumento en los niveles de colesterol en sangre, especialmente del colesterol transportado por lipoproteínas de baja densidad (c-LDL). Su prevalencia en la población es bastante frecuente, al detectarse en al menos 1 caso por cada 250 personas en la población general, y habiendo 200.000 personas en España con este diagnóstico.
De esta manera, esta patología genética, que se transmite al 50% de la descendencia y aparece desde el nacimiento, sigue siendo un problema de salud pública poco reconocido y mal gestionado, según la Fundación Hipercolesterolemia Familiar (FHF). Por lo que la detección precoz se considera una estrategia coste-eficaz para reducir la carga de morbilidad cardiovascular asociada a la enfermedad.
Sin embargo, un equipo internacional ha dado un paso decisivo en la lucha contra esta enfermedad al presentar una estrategia innovadora para tratar el colesterol alto que prescinde de los métodos tradicionales y promete alternativas para los pacientes sin respuesta a las terapias actuales. Esta investigación, publicada recientemente por la Universidad Médica de Carolina del Sur (MUSC) en la revista Communications Biology, introduce un enfoque que podría transformar el tratamiento de uno de los trastornos hereditarios más frecuentes a escala global.
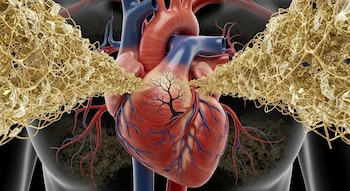
Un nuevo enfoque: atacar la producción desde el origen
En individuos sanos, el receptor de lipoproteínas de baja densidad (LDLR) actúa como un anclaje en el hígado, permitiendo que el colesterol se degrade y elimine del organismo. Las personas con hipercolesterolemia familiar presentan mutaciones que inutilizan este mecanismo, lo que provoca una acumulación silente y prolongada de colesterol que puede desembocar en infartos y otras enfermedades cardiovasculares. El modo clásico de abordar la HF ha sido el uso de estatinas, medicamentos que aumentan la actividad del receptor de LDL y favorecen la eliminación del colesterol circulante, determinan en Scitech Daily.
No obstante, esta vía tiene serias limitaciones: los pacientes con mutaciones graves en ambos genes del LDLR apenas responden a las estatinas, quedando expuestos a complicaciones a largo plazo, asegura Stephen Duncan, principal responsable del estudio. Ante este problema, los investigadores de la MUSC proponen invertir el razonamiento, es decir, en vez de potenciar la eliminación, buscar una intervención en la formación de las partículas que transportan el colesterol. El foco se traslada a la apolipoproteína B (apoB), una proteína indispensable para la creación de las partículas de LDL.
Sin apoB, el colesterol no logra formar las estructuras necesarias para circular en la sangre. Por tanto, atacar la producción de apoB permite reducir la cantidad de colesterol que entra en el torrente sanguíneo, sin depender del receptor alterado en estos pacientes. Para probar esta teoría, el equipo utilizó células madre pluripotentes inducidas (iPSC), reprogramadas a partir de células adultas para que adquieran propiedades similares a las del hígado humano. Esta estrategia permitió simular con precisión el metabolismo del colesterol en humanos y superar las diferencias que existen al emplear modelos animales.

Los investigadores analizaron más de 130.000 moléculas de la Colección de Compuestos de Carolina del Sur (SC3) y detectaron un grupo que lograba disminuir de manera significativa la liberación de apoB, junto con una reducción de los triglicéridos y el colesterol dentro de las células. El propio Duncan explicó: “Nuestro enfoque es la forma original de hacer farmacología: intentar encontrar fármacos que puedan curar la enfermedad sin saber cómo lo hacen. Se modela la enfermedad y luego se prueban fármacos para descubrir cuáles funcionan. Después, se puede determinar retrospectivamente cómo funciona el fármaco”.
Ratones “Avatar”: superando las limitaciones de los modelos animales
El avance enfrentó un obstáculo al pasar a pruebas en ratones: las células hepáticas murinas no respondieron igual que las humanas, y los compuestos no demostraron el mismo potencial. Para sortear esta barrera, los investigadores usaron los llamados ratones “Avatar”, desarrollados por la empresa Yecuris. Estos animales han sido modificados genéticamente para portar células hepáticas humanas, lo que les otorga un metabolismo del colesterol similar al de las personas. En ellos, los compuestos seleccionados lograron reducir los niveles de lípidos conforme a lo esperado, reforzando la hipótesis de que podrían convertirse en tratamientos efectivos para la HF.
Uno de los puntos más relevantes de esta estrategia es que la acción de los compuestos identificados no depende del receptor de LDL, lo que representa una esperanza para quienes no responden a las terapias habituales. Esta línea también marca un cambio conceptual: en vez de adaptar los tratamientos a los sistemas animales, se utiliza tecnología de células madre para modelar la enfermedad en sistemas humanos desde el inicio.
La investigación se ha extendido además con un estudio publicado en 2026 en microPublication Biology, que ha analizado el impacto del compuesto principal, DL-1, sobre la actividad genética de las células hepáticas humanas. Los resultados mostraron que el tratamiento alteró la expresión de 182 genes, y que la mayoría de los cambios no afectaron las funciones biológicas principales del hígado. Los científicos observaron un aumento en los genes de metalotioneína, encargados de regular los metales y proteger las células frente al estrés. Este patrón podría estar asociado a la interacción entre la estructura tiólica del compuesto y los iones metálicos intracelulares.
De este modo, los análisis sugieren que el DL-1 no actúa desactivando el gen de apoB, sino que interfiere en el procesamiento y la secreción de la proteína, permitiendo una reducción selectiva y precisa de las partículas de LDL. Los próximos desafíos incluyen determinar la seguridad a largo plazo de estos compuestos y explorar su combinación con tratamientos existentes, como las estatinas.
Últimas Noticias
Los jóvenes dedican casi la mitad de su salario a alquilar una habitación: “Eso no es independencia es supervivencia”
Las rentas en pisos compartidos se disparan en las grandes ciudades como Madrid y Barcelona, donde un cuarto supera los 600 euros mensuales

Los expertos en vino eligen los mejores del mercado: blancos, tintos y rosados de premio, algunos por menos de 6 euros
El Salón Gourmets 2026 ha celebrado la 41.ª edición de los premios Guía Vinos Gourmets, un concurso que reconoce la excelencia del sector vinícola español y a sus vinos, bodegas, profesionales e instituciones

Receta de flan de café: un postre cremoso y muy fácil para triunfar en la sobremesa
Su textura cremosa y el delicado aroma a café lo convierten en una opción irresistible para acabar una comida entre amigos

Acalasia, la enfermedad que impide que los alimentos lleguen al estómago y que puede confundirse con el reflujo: síntomas y tratamiento
Esta patología poco frecuente está relacionada con un daño en los nervios del esófago
Resultados del Super Once del 16 abril
Como cada jueves, aquí están los números ganadores del sorteo dado a conocer por Juegos Once




