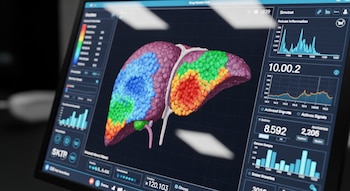
Si los científicos pudieran reducirse a tamaño microscópico y viajar a través del cuerpo humano, como la tripulación del submarino en el clásico de ciencia ficción de 1966, Viaje fantástico, sin duda una de sus primeras paradas sería el hígado.
La estructura única de nuestro órgano interno más grande se compone de pequeñas unidades funcionales hexagonales llamadas lobulillos, cada una de las cuales realiza más de 500 funciones simultáneamente. Estudios de las décadas de 1970 y 1980 revelaron que las células hepáticas se reparten estas numerosas tareas, según su ubicación dentro de cada subunidad. Sin embargo, la tecnología disponible en aquel entonces solo proporcionaba una imagen borrosa de esta división del trabajo.
En un nuevo estudio publicado en Nature, científicos del Instituto Weizmann de Ciencias, junto con colegas del Centro Médico Sheba y la Clínica Mayo, presentan el primer atlas genético de un hígado humano sano con una resolución de 2 micras.
Los hallazgos demuestran que la división del trabajo en el hígado humano difiere de la de otros mamíferos y es más extensa de lo que se creía, lo que ayuda a explicar por qué ciertas regiones del hígado son particularmente vulnerables a la enfermedad del hígado graso.
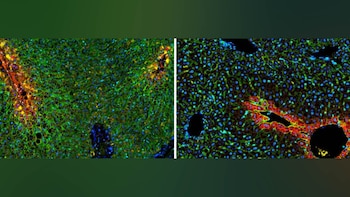
En los últimos años, los avances tecnológicos han permitido identificar qué genes están activos en cada célula individual, así como mapear las posiciones espaciales precisas de las células dentro del tejido. Sin embargo, un mapa completo de la división funcional en el hígado humano seguía siendo difícil de obtener, principalmente debido a la dificultad de conseguir muestras de tejido de donantes sanos.
Investigadores del grupo del Prof. Shalev Itzkovitz en el Instituto Weizmann se dieron cuenta de que la solución podría provenir de la donación altruista de hígado en vida. Dado que el hígado tiene una notable capacidad de regeneración, las personas sanas pueden donar una parte sustancial de su hígado a pacientes que lo necesitan.
Con la ayuda del Prof. Ido Nachmany y el Prof. Niv Pencovich del Departamento de Cirugía General y Trasplante del Centro Médico Sheba, y el Dr. Timucin Taner de la Clínica Mayo en Minnesota, los investigadores obtuvieron ocho muestras de hígado de donantes sanos y construyeron un atlas de expresión génica del hígado humano.

“Se ha descubierto que miles de genes se activan a distintos niveles en las células hepáticas de diversas localizaciones, lo que apunta a una organización interna mucho más precisa y compleja de lo que se creía”, afirma Itzkovitz.
“En lugar de la división burda en tres zonas funcionales que se ha aceptado durante décadas, el atlas revela ocho regiones con funciones distintas. Este mapeo preciso permite ahora a cualquier laboratorio del mundo profundizar en el estudio del hígado e investigar por qué diferentes regiones son susceptibles a distintas enfermedades”, explica.
Y agrega: "Las enfermedades metabólicas, por ejemplo, tienden a originarse en el centro del lobulillo, mientras que las inflamaciones virales y autoinmunes aparecen principalmente en su periferia. Del mismo modo, el cáncer de hígado y las metástasis de otros tipos de cáncer tienen sus localizaciones preferidas. La clave para comprender estos patrones reside en los datos genéticos detallados que hemos recopilado”.
Para permitir la comparación con otras especies, el laboratorio de Itzkovitz también analizó hígados sanos en ratones, así como en mamíferos más grandes (cerdos y vacas), cuyas tasas metabólicas y tamaños de lóbulos son similares a los de los humanos.
En todos los mamíferos, la sangre fluye a través del lóbulo desde la periferia hacia el centro, suministrando oxígeno y nutrientes a las células a lo largo del camino. Como resultado, la periferia se caracteriza por una abundancia de recursos, mientras que el centro experimenta una escasez relativa.
En todos los mamíferos estudiados, excepto en los humanos, estas condiciones de agotamiento en el centro del lóbulo dieron como resultado una actividad celular relativamente menor. En los humanos, sin embargo, se descubrió que el núcleo del lóbulo realiza numerosas funciones, incluyendo la síntesis de grasas a partir del exceso de energía, la producción de glucosa a partir de fuentes no carbohidratadas durante el ayuno, el filtrado de toxinas y la secreción de bilis para facilitar la digestión.
Otra diferencia notable entre el hígado humano y el de otros mamíferos radica en el almacenamiento de glucosa. El hígado funciona como el “depósito de combustible” del cuerpo, absorbiendo eficientemente los azúcares durante las comidas y liberándolos de forma controlada entre ellas. El estudio reveló que, en los humanos, la captación de glucosa se produce principalmente en el centro de los lóbulos, en lugar de en su periferia, a diferencia de lo que ocurre en los ratones.
“Esta división del trabajo es a la vez una bendición y una maldición”, explicó Itzkovitz. “Permite que el hígado almacene carbohidratos de manera eficiente: las células del centro del lóbulo absorben y almacenan glucosa directamente de la sangre, mientras que las células de la periferia convierten el lactato en glucosa, contribuyendo así a las reservas de energía utilizadas durante el ayuno. Sin embargo, este sistema eficiente no fue diseñado para una dieta moderna rica en grasas y carbohidratos, lo que podría explicar por qué tendemos a acumular exceso de grasa en el hígado y a desarrollar fibrosis hepática”, añadió.

Para hacer frente al desgaste celular y prevenir enfermedades, parece haber evolucionado un mecanismo de renovación único en el centro del lóbulo hepático humano. “Descubrimos que en los humanos, a diferencia de otros mamíferos, un tipo particular de célula inmunitaria prefiere residir en el centro del lóbulo en lugar de proteger su periferia, el punto de entrada de la sangre al tejido”, remarcó el Dr. Oran Yakubovsky, del laboratorio de Itzkovitz, quien dirigió el estudio y también es residente de cirugía en el Centro Médico Sheba.
“Las células de Kupffer son células fagocíticas especializadas que ofrecen protección contra infecciones, pero también engullen, descomponen y reciclan los restos de células desgastadas. Nuestra hipótesis es que en los humanos se ‘reubicaron’ en el centro para hacer frente al aumento del desgaste celular que se produce allí“, indicó.
En la parte final del estudio, los científicos demostraron cómo su nuevo atlas puede utilizarse para rastrear el desarrollo de enfermedades. Se centraron en la enfermedad del hígado graso asociada a la disfunción metabólica, una afección común vinculada a la obesidad y la diabetes, en la que la grasa se acumula en el hígado y puede provocar inflamación y fibrosis.
La comparación de células hepáticas sanas con aquellas que habían comenzado a acumular grasa reveló una respuesta protectora: las células que empezaron a acumular grasa desactivaron genes implicados en la producción y absorción de grasa, mientras que activaron genes asociados a su descomposición. Sin embargo, el hígado humano tiene una limitación que reduce la eficiencia de este proceso: la acumulación de grasa también conlleva una disminución en la producción de ciertos componentes de las mitocondrias, los orgánulos responsables de la descomposición de las grasas.

“Gracias al mapeo preciso del hígado, podría ser posible desarrollar tratamientos dirigidos a los genes responsables de la vulnerabilidad de ciertas regiones a determinadas enfermedades”, afirmó Itzkovitz.
“Además, el método de crear un atlas genético con resolución unicelular a partir de muestras de donantes sanos puede aplicarse a otros órganos que aún no se han mapeado con precisión en humanos. Esto podría cambiar radicalmente nuestra comprensión de la estructura y la función del cuerpo humano”, concluyó.
También participaron en el estudio el Dr. Keren Bahar Halpern, Sapir Shir, Roy Novoselsky, el Dr. Adi Egozi, el Dr. Tal Barkai, el Dr. Yotam Harnik, el Dr. Amichay Afriat y la Dra. Yael Korem Kohanim del Departamento de Biología Celular Molecular de Weizmann; Dr. Chen Mayer y Dr. Ron Pery del Centro Médico Sheba, Tel Hashomer; Dr. Rouven Hoefflin de la Universidad de Friburgo, Alemania; Ofra Golani, Dra. Inna Goliand, Dr. Yoseph Addadi, Dr. Merav Kedmi y Dr. Hadas Keren-Shaul del Departamento de Instalaciones Centrales de Ciencias Biológicas de Weizmann; y la Dra. Liat Fellus-Alyagor, Lena Prichislov y Dana Hirsch del Departamento de Recursos Veterinarios de Weizmann.
*Este contenido fue producido por expertos del Instituto Weizmann de Ciencias, uno de los centros más importantes del mundo de investigación básica multidisciplinaria en el campo de las ciencias naturales y exactas, situado en la ciudad de Rejovot, Israel.
Últimas Noticias
La ciencia identifica hábitos que preservan y mejoran la agilidad mental
Cuáles son los cambios en el estilo de vida que pueden marcar la diferencia en el funcionamiento cerebral, según investigaciones recientes

¿Por qué el estrés engorda? La explicación de los expertos sobre la conexión hormonal
La exposición prolongada a situaciones de tensión eleva el cortisol. Cómo detectar si es hambre real o emocional

Hígado graso: se duplicaron las consultas en los últimos cinco años
La acumulación anormal de grasa vinculada al sobrepeso, la obesidad y la diabetes tipo 2 impulsa un crecimiento inédito en la demanda de atención médica, según expertos del Hospital de Clínicas de la UBA
Qué es el “efecto overview”, el cambio mental que viven los astronautas al volver del espacio
Observar la Tierra desde la órbita lunar provoca un cambio profundo. Tres especialistas le explican a Infobae cómo esta experiencia redefine la percepción y las prioridades tras el regreso

Cuánta agua necesita un planeta para ser habitable: el estudio que redefine la búsqueda de vida en el universo
Una investigación de la University of Washington determinó que no alcanza con la presencia de océanos: se requiere un volumen mínimo para sostener procesos geológicos que estabilicen el clima. El hallazgo descarta a muchos mundos secos como candidatos viables para albergar organismos


