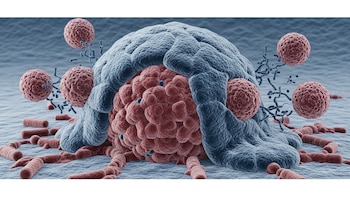
Un sistema de “vientos” internos en las células fue identificado por un equipo de científicos, lo que permitió descubrir un mecanismo que impulsa el transporte de proteínas y podría transformar la comprensión sobre la diseminación del cáncer y la reparación de tejidos.
La investigación, publicada en la revista científica Nature Communications y difundida por el medio especializado en divulgación científica Science Daily, demuestra que las células generan corrientes internas dirigidas que aceleran su movimiento y desafían los principios aceptados en la biología molecular.
La clave de este hallazgo radica en la observación de que las células no dependen únicamente del movimiento aleatorio para distribuir proteínas en su interior. Según la información, el trabajo liderado por los investigadores de la Oregon Health & Science University (OHSU) descubrió que existen flujos de fluido similares a los vientos alisios, capaces de transportar proteínas esenciales, como la actina, con una velocidad muy superior a la atribuida previamente a la difusión al azar.
Este sistema, denominado por los científicos como “pseudo-orgánulo”, no está delimitado por una membrana, pero cumple una función clara al organizar el comportamiento y la dirección del transporte intracelular. La existencia de una barrera de actina-miosina en la parte frontal de la célula, según los experimentos, permite que estos flujos actúen como ríos internos que llevan proteínas hacia el área de avance. Esta región, separada físicamente del resto del citoplasma, dirige los componentes necesarios para que la célula se extienda, adhiera, repare tejidos y coordine respuestas inmunes.
Hasta este descubrimiento, la enseñanza en biología sostenía que las proteínas se desplazaban a través de difusión, un proceso aleatorio y lento. James Galbraith, doctor en biología celular y coautor del estudio, explicó: “Nos dimos cuenta de que los modelos de los libros de texto ignoraban una parte fundamental. Debe existir algún tipo de flujo intracelular que empuje las proteínas hacia adelante”.
El experimento inesperado que desafió el modelo clásico
El primer indicio del fenómeno surgió durante una clase de neurobiología en el Marine Biological Laboratory de Massachusetts. Según relató Catherine Galbraith, doctora en biología celular y coautora, mientras realizaban una práctica con estudiantes, observaron una banda oscura en la zona frontal de las células vivas.
Al emplear un láser para volver invisibles las proteínas en una franja trasera y así rastrear su movimiento —una técnica habitual—, detectaron que una ola de actina soluble era empujada abruptamente hacia adelante.
A partir de esa observación casual, el equipo de la OHSU, que cuenta con experiencia en microscopía avanzada por su colaboración con el Nobel Eric Betzig en el Janelia Research Campus de Virginia, recurrió a novedosos métodos de imagen para verificar sus hipótesis.
Uno de estos, denominado FLOP (Fluorescence Leaving the Original Point), permitió activar moléculas fluorescentes en un punto específico y monitorizar su desplazamiento, una innovación que los propios investigadores describieron como todo lo contrario a un fallo: “No fue para nada un flop, porque funcionó”, sentenció Catherine.
La colaboración con expertos en espectroscopía de correlación de fluorescencia y técnicas como la iPALM (Interferometric PhotoActivated Localization Microscopy), que puede resolver estructuras a nanoescala, permitió confirmar visualmente la existencia de compartimentos funcionales antes invisibles.
El “motor” del avance: de la célula normal al cáncer agresivo
Mediante este mecanismo, las células pueden comprimir selectivamente su región trasera —de modo similar a exprimir una esponja— y dirigir el flujo de material justo hacia donde lo necesitan.
Los flujos, lejos de ser específicos para una sola proteína, transportan simultáneamente numerosos tipos, lo que convierte al sistema en una herramienta eficiente para todos los procesos celulares que requieren rapidez, como el cambio de forma, la migración o la reparación después de una lesión.
Los investigadores advirtieron que esta capacidad de movilizar proteínas con velocidad y dirección podría ser determinante en el comportamiento agresivo de ciertos tipos de células cancerosas. “Sabemos que estas células altamente invasivas poseen este mecanismo que les permite enviar muy rápidamente las proteínas necesarias a la parte delantera”, explicó James Galbraith, quien agregó: “Todas las células tienen componentes similares, pero el resultado final depende de cómo se ensamblan”.
Este planteamiento sugiere que la diferencia en la organización y uso de estos “vientos” celulares podría ser clave en la invasividad de los tumores. Los autores consideran que entender esta distinción abriría el camino para terapias dirigidas que desaceleren o detengan la propagación del cáncer, mediante la intervención en el sistema de transporte intracelular sin afectar las funciones de las células sanas.
Repercusiones para la medicina y la biología sintética
La descripción de esta dinámica como un “pseudo-orgánulo” implica una revisión del marco clásico sobre la arquitectura celular. Esto abre el interés hacia campos tan variados como la biología de sistemas, el diseño de fármacos, la ingeniería de tejidos y la biología sintética.
El hallazgo, según los autores, fue posible gracias a la confluencia de disciplinas —ingeniería, física, microscopía avanzada y biología celular— y a los recursos únicos del Janelia Research Campus. “Todo lo que hacía falta era mirar. Los flujos siempre estuvieron ahí. Ahora sabemos cómo los utilizan las células”, puntualizó Catherine Galbraith.
Últimas Noticias
Un marcador digital cerebral durante el sueño se asocia con mayor riesgo de demencia
Un estudio internacional observacional en más de 7.000 adultos halló que una edad del cerebro superior a la cronológica, calculada mediante inteligencia artificial a partir de electroencefalografía durante el sueño, se asocia con un mayor riesgo futuro de deterioro cognitivo
El uso de inteligencia artificial revela rutas cerebrales secuenciales durante el procesamiento de información
El método desarrollado en Stanford University establece cuándo y dónde se producen respuestas neuronales, proporcionando una herramienta clave para anticipar alteraciones en el cerebro y personalizar terapias, según la dinámica de cada paciente
La actividad manual se consolida como herramienta para reducir ansiedad y depresión, según expertos
Diversos estudios confirman los beneficios de prácticas creativas como pintar, bordar o coser para la salud mental

Cómo un ultrasonido en la amígdala cambia nuestra reacción emocional
Científicos comprobaron que influir de manera puntual en este centro cerebral altera la forma en que interpretamos señales ambiguas, ofreciendo esperanza para abordar la ansiedad o la depresión

Las células dendríticas revitalizadas logran frenar tumores, según una investigación
Un estudio en ratones mostró que mejorar el metabolismo de estas unidades del sistema inmunitario permite potenciar los tratamientos oncológicos más avanzados