
Inicialmente, la pandemia COVID-19 se consideró una enfermedad pulmonar exclusiva, que eventualmente condujo a síntomas respiratorios graves. Mientras tanto, la acumulación de estudios experimentales y clínicos ha sugerido que el SARS-CoV-2 también puede causar lesiones en los riñones, el corazón, el cerebro y los órganos gastrointestinales y endocrinos.
La diabetes preexistente es una comorbilidad altamente prevalente observada en el 22% de los pacientes y, como tal, aumenta el riesgo de una enfermedad grave, requiriendo más intervenciones y aumento de la mortalidad. En segundo lugar, la infección por SARS-CoV-2 parece afectar el páncreas exocrino, manifestándose como pancreatitis en el 32,5% de los pacientes críticos, y agrandamiento pancreático y niveles anormales de amilasa o lipasa en el 17% de los pacientes. En tercer lugar, se ha observado una desregulación metabólica en pacientes con COVID-19 como: aumento de la hiperglucemia en pacientes con diabetes tipo 2; cetoacidosis en el 6,4% de los pacientes diabéticos y no diabéticos y en estudios de casos que informan cetoacidosis sobre la infección por SARS-CoV-2, acompañada de diabetes mellitus tipo 1 de nueva aparición (T1DM) en ausencia de autoanticuerpos.
PUBLICIDAD
En un estudio de cohorte de pacientes con diabetes, se notificó hiperglucemia en más del 50% de todos los casos y casi un tercio experimentó cetoacidosis diabética 29 . Finalmente, un estudio multicéntrico encontró un aumento del 80% de la DM1 de nueva aparición en los niños durante la pandemia de COVID-19. Un metaanálisis reciente resume que el COVID-19 grave se asocia con un aumento de los niveles de glucosa en sangre. Sin embargo, la prueba formal del SARS-CoV-2 como un virus trópico de células β, que potencialmente conduce a la diabetes, aún no existe, y la única evidencia correlativa se mantiene a la luz de hallazgos experimentales y clínicos contradictorios. Se justifican los resultados agudos y a largo plazo recopilados prospectivamente sobre casos de diabetes de nueva aparición, junto con interpretaciones reflexivas de los datos emergentes hasta la aclaración final de este debate.
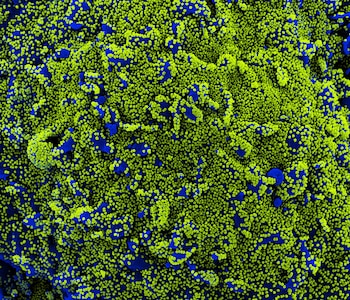
Ese fue el foco en el que se centró un estudio llevado adelante por un equipo del Instituto de Virología Molecular de la Universidad de Ulm, Alemania. En él definieron patrones de expresión de ACE2 y TMPRSS2 en tipos de células pancreáticas endocrinas y exocrinas humanas, emplearon cultivos de islotes pancreáticos humanos para demostrar la susceptibilidad a la infección por SARS-CoV-2 y la replicación viral en células β y demostraron que la infección por SARS-CoV-2 afecta la secreción de insulina estimulada por glucosa (GSIS). Además, visualizaron partículas virales que se replican en las células pancreáticas endocrinas y definieron sus patrones de localización subcelular y finalmente presentaron ejemplos de patrones de infección multiorgánica, incluido el páncreas de pacientes que murieron por COVID-19.
PUBLICIDAD
Una pareja imperfecta

Según el estado actual de los conocimientos, la expresión de ACE2 sigue siendo el principal determinante de la entrada del SARS-CoV-2 y, por tanto, del tropismo de los órganos. Varias proteasas pueden cebar la proteína S del coronavirus, cuya expresión de TMPRSS2 pancreática también coincidió con el patrón de infección de pacientes fallecidos por COVID-19 incluidos en el análisis. Los investigadores detectaron que ACE2 y TMPRSS2 se colocalizan menos con marcadores de células δ y α. Sin embargo, esta menor frecuencia no excluye la infección como sugieren los datos previos.
PUBLICIDAD
Sin embargo, independientemente de un posible debate sobre la expresión de la proteína de entrada viral, observaron una infección productiva por SARS-CoV-2 de islotes cultivados ex vivo utilizando ensayos de última generación basados en virología molecular, lo que proporciona evidencia de la presencia de entrada funcional factores.
La observación más llamativa fue un compartimiento intermedio ER-Golgi agrandado y vacuolizado, similar a las observaciones en células epiteliales intestinales, renales y de las vías respiratorias infectadas con SARS-CoV-2. Las características distintivas de la diferenciación endocrina, es decir, los gránulos secretores, se desplazan y reducen significativamente. Sin embargo, se requiere un análisis basado en TEM más completo a lo largo de un ciclo de replicación viral completo en islotes humanos, así como más muestras de pacientes infectados, para sacar conclusiones definitivas. Sin embargo, las observaciones de TEM están en línea con la secreción de insulina afectada observada en el presente estudio, a pesar de que se enfrentaron variaciones experimentales en las cuatro preparaciones de islotes investigadas.
PUBLICIDAD

Los resultados muestran que la replicación viral en islotes infectados ex vivo fue inhibida de manera eficiente por remdesivir usado como control para prevenir la replicación del SARS-CoV-2. Esta inhibición de la replicación viral no se asoció con un rescate completo en la función de las células β ni con la restauración completa de los transcriptomas. Lo más probable, argumentan los especialistas, es que esto se deba a un retraso en la recuperación total de las células β, que no se puede alcanzar en el contexto experimental actual debido al deterioro de los islotes en el cultivo prolongado ex vivo. Sin embargo, los efectos del remdesivir sugieren que los cambios observados son específicos de la infección por SARS-CoV-2.
La investigación del páncreas de las personas fallecidas por COVID-19 reveló una distribución dispersa de grupos de células infectadas a lo largo del órgano en todos los pacientes, más visible en el compartimento exocrino, pero cerca de los islotes de Langerhans. Tal patrón podría indicar la propagación a las células pancreáticas vecinas que se originan a partir de unas pocas células infectadas, a las que pueden llegar las partículas virales directamente a través del torrente sanguíneo durante la viremia temporal, que ocurre típicamente en el COVID-19 grave
PUBLICIDAD
Para los especialistas, específicamente, la insulina podría no ser un marcador adecuado para mostrar la colocalización con proteínas virales. Por tanto, la estimación de las tasas de infección de las células respectivas, dentro de los islotes o tejidos pancreáticos, sigue siendo un desafío. Aún se justifica el patrón preciso de infección por SARS-CoV-2 en subpoblaciones de islotes humanos, y queda por determinar si el número de células infectadas con SARS-CoV-2 y la pérdida de identidad asociada de las células β son suficientes para afectar la función endocrina en islotes sanos y enfermos.
En consecuencia, los resultados de este documento plantean la pregunta de si el SARS-CoV-2 perturba directamente la integridad de las células β y potencialmente conduce a una desregulación endocrina y causa T1DM autoanticuerpo negativo, como se informó en estudios clínicos recientes después de la infección por cronavirus. Alternativamente, la infección por SARS-CoV-2 podría ser un factor desencadenante de la diabetes mellitus autoinmune que surge incluso años después de la recuperación, lo que respalda la necesidad de un seguimiento a largo plazo de los pacientes con COVID-19.
PUBLICIDAD
SEGUÍ LEYENDO:
PUBLICIDAD
PUBLICIDAD
PUBLICIDAD
PUBLICIDAD
Últimas Noticias
Los nuevos 60: los cambios en la dieta adulta que pueden agregar casi 10 años de vida
Los cambios en la dieta en la edad adulta pueden agregar casi 10 años de vida según un amplio estudio científico. Una guía de pequeños grandes hábitos para alcanzar la plenitud

9 tips para comenzar a hacer deporte y mejorar el estado físico
Una guía para evitar las excusas y ponerse en movimiento. Incorporar desafíos de manera paulatina y armar una rutina son los pasos claves para empezar

Día Mundial del Pene: cuidados para la higiene adecuada y consejos para prevenir el cáncer y otras enfermedades
La fecha busca celebrar la fertilidad y generar conciencia acerca de la práctica del sexo seguro. La salud y el cuidado del órgano reproductor masculino son fundamentales para mantener una vida sexual plena y saludable

Turbulencias durante el vuelo: cinco consejos para subirse al avión sin miedo
Un piloto comercial explica por qué son habituales estos movimientos, además brindó recomendaciones sobre qué asiento elegir para sufrir menos durante el viaje. Una guía práctica y sencilla sobre algunos de los puntos más consultados por los pasajeros

Cuáles son los tres desayunos ideales para personas con diabetes e hipertensión
Las clásicas tostadas con mermelada pueden reemplazarse por opciones más saludables, con más proteínas, fibras y minerales. Cómo ayudan a controlar estas enfermedades



