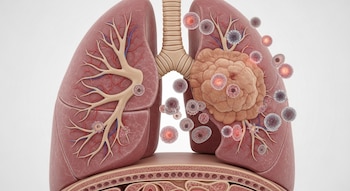
Investigadores de Mayo Clinic identificaron un mecanismo que permite a ciertos tumores de cáncer de pulmón debilitar la respuesta del sistema inmune, un fenómeno que podría explicar por qué muchos pacientes no responden plenamente a tratamientos innovadores como la inmunoterapia. El estudio, que se realizó en modelos animales, fue publicado en la revista Cancer Immunology Research.
Cuando el sistema de defensa se vuelve vulnerable
El cáncer de pulmón continúa siendo la principal causa de muerte a nivel global. Según estimaciones de la Organización Mundial de la Salud (OMS), en 2022 se diagnosticaron 2,48 millones de nuevos casos y se registraron 1,8 millones de muertes por esta enfermedad en todo el mundo.
En los últimos años, la inmunoterapia —tratamientos que activan las defensas inmunológicas para identificar y eliminar células tumorales— representó un cambio importante en el abordaje de esta enfermedad. Sin embargo, la respuesta clínica sigue siendo desigual.
Una de las razones radica en los linfocitos T reguladores, células cuya función natural es evitar que el sistema inmune reaccione de forma excesiva y dañe tejidos sanos. En condiciones normales, estas células actúan como un freno de seguridad que mantiene el equilibrio defensivo del organismo.
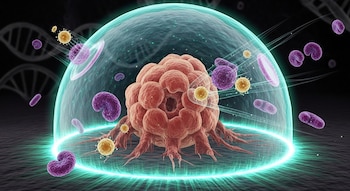
El problema surge cuando el tumor logra utilizar ese mismo mecanismo para protegerse. “Se apropia de un sistema diseñado para proteger al organismo y lo utiliza a su favor”, explicó Henrique Borges da Silva, inmunólogo de Mayo Clinic y autor principal del estudio.
El receptor P2RX7 y el “camuflaje” tumoral
El análisis de datos de pacientes con cáncer de pulmón no microcítico (el tipo más común de cáncer de pulmón, diferente al de células pequeñas) reveló que los linfocitos T reguladores dentro del tumor presentan niveles elevados del receptor P2RX7. Esta mayor expresión se asocia a peores perspectivas de supervivencia.
La proteína actúa como un sensor que detecta ATP, una molécula liberada por células sometidas a estrés o daño. En el entorno tumoral, esta sustancia se encuentra en altas concentraciones, lo que atrae y activa a los linfocitos T reguladores.

Puede pensarse este proceso como si el tumor emitiera señales que convocan a células encargadas de reducir la respuesta inmunitaria. Al llegar, estas células disminuyen la vigilancia del sistema defensivo, lo que facilita que el tumor crezca y se expanda con menor resistencia.
Qué ocurre cuando se bloquea la proteína
Para comprender mejor el fenómeno, los investigadores realizaron experimentos en modelos animales. Al eliminar el receptor P2RX7 de los linfocitos T reguladores, detectaron un crecimiento tumoral más lento y una mayor presencia de células inmunitarias capaces de atacar el cáncer.
Además, el bloqueo de este receptor potenció la cooperación entre distintos componentes del sistema inmune, lo que favoreció la producción de anticuerpos y la organización de estructuras inmunológicas dentro del tumor, factores asociados a mejores resultados clínicos.

Otro hallazgo relevante fue la relación entre P2RX7 y la molécula CTLA-4, un conocido freno inmunitario. Sin el receptor, los linfocitos T reguladores presentaron niveles menores de esta molécula y una capacidad reducida para suprimir la respuesta defensiva.
En una etapa posterior, el equipo evaluó un fármaco experimental capaz de inhibir P2RX7. Los resultados mostraron una reducción del tamaño tumoral y una menor acumulación de linfocitos T reguladores en el microambiente del cáncer.
Aunque el medicamento aún no está aprobado para uso clínico, los datos sugieren que podría utilizarse en el futuro en combinación con inmunoterapias existentes. La estrategia buscaría potenciar la respuesta inmunitaria al mismo tiempo que se desactiva el mecanismo que el tumor utiliza para evadirla.
Comprender la resistencia para ampliar las opciones terapéuticas

Los especialistas subrayan que uno de los mayores desafíos actuales en oncología es entender por qué la inmunoterapia funciona en algunos pacientes y no en otros. Este hallazgo aporta una pieza clave al mostrar cómo los tumores pueden manipular células del propio sistema inmunitario para sobrevivir.
Más allá de su relevancia clínica, el estudio también refuerza la idea de que el cáncer no es solo un conjunto de células que crecen sin control, sino un ecosistema complejo donde interactúan el tumor, el sistema inmune y el entorno celular.
Si futuras investigaciones confirman estos resultados en humanos, el receptor P2RX7 podría convertirse en un nuevo objetivo terapéutico capaz de mejorar la eficacia de tratamientos actuales y ofrecer alternativas para pacientes con respuesta limitada.
En un escenario donde la inmunoterapia continúa evolucionando, comprender y bloquear los mecanismos de evasión tumoral representa un paso fundamental para avanzar hacia terapias más efectivas y personalizadas.
Últimas Noticias
Los beneficios para la salud de la cúrcuma y el jengibre, respaldados por la ciencia
Ambas raíces mejoran la función intestinal, contribuyen a la protección celular y pueden aliviar dolores articulares y musculares. Cómo utilizarlas en la cocina

Cuál es el fungicida que podría causar enfermedades hereditarias en animales durante 20 generaciones
El estudio, publicado en Proceedings of the National Academy of Sciences, demostró que este agroquímico utilizado en cultivos puede provocar daños biológicos y metabólicos que se transmiten a la descendencia, incluso en ausencia de contacto directo. Qué puede ocurrir en los humanos
Por qué el dolor crónico puede durar más en mujeres, según un nuevo estudio
Una investigación de la Michigan State University demostró que la producción de una molécula antiinflamatoria clave es mayor en hombres, lo que provoca que el dolor persista durante menos tiempo. Los deatalles

Qué son los ejercicios cognitivos digitales y cómo pueden mejorar las funciones cerebrales tras una lesión traumática
Un estudio de la New York University revela que la neuroplasticidad puede estimularse a través de prácticas computarizadas. Cómo logra generar mejoras estructurales y funcionales, incluso años después del incidente
¿Cuántos minutos tiene febrero? Un juego de multiplicación
Una curiosa relación matemática revela cómo contar el mes con ingenio y sorprende a quienes disfrutan de los dilemas lógicos