
Investigadores de la UNAM han desarrollado la molécula GK-1, una terapia innovadora que podría transformar el tratamiento del cáncer de mama triple negativo.
Según Ciencia UNAM-DGDC, los estudios en modelos animales muestran una reducción clara en el tamaño de tumores y en la metástasis.
Actualmente, el equipo de investigación del Instituto de Investigaciones Biomédicas de la Universidad Nacional Autónoma de México (UNAM) se encuentra preparando el inicio de ensayos clínicos en humanos.
Cuál es el cáncer de mama triple negativo
El cáncer de mama triple negativo es una de las formas más agresivas de esta enfermedad, con opciones terapéuticas muy limitadas.
Las pacientes suelen enfrentar tumores que se vuelven resistentes a los tratamientos actuales y que desarrollan mutaciones que dificultan su control médico.
¿Por qué esta molécula podría modificar el futuro de los tratamientos contra cáncer de mama?
La doctora Edda Sciutto y la doctora Gladis Fragoso lideran la investigación sobre GK-1, un compuesto desarrollado y estudiado durante más de veinte años.
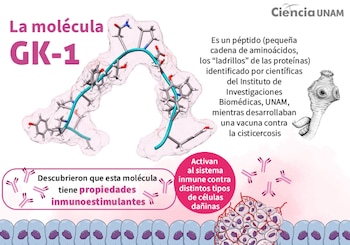
Esta molécula fue identificada inicialmente en la búsqueda de una vacuna contra la cisticercosis y, con el tiempo, demostró ser un inmunoestimulante capaz de activar al sistema inmune contra células dañinas, incluyendo las cancerosas.
Los ensayos preclínicos en ratones revelaron que la aplicación de GK-1 disminuyó de forma significativa el tamaño de los tumores y la aparición de metástasis en diferentes órganos.
También se constató un aumento en la actividad de linfocitos citotóxicos (CD8+), especializados en eliminar tejidos malignos.
De acuerdo con Ciencia UNAM-DGDC, estos resultados refuerzan la posibilidad de que GK-1 beneficie a personas con cáncer de mama triple negativo.
El equipo investigativo ya completó la formulación de GK-1 para su administración subcutánea, como parte de los preparativos para su uso en humanos.
Además, en la Facultad de Medicina Veterinaria y Zootecnia de la UNAM se realizaron estudios en perros con cáncer oral avanzado y sin otras opciones terapéuticas, evaluando el potencial terapéutico del compuesto.
Qué tan segura y efectiva es la molécula GK-1

En esos estudios, las investigadoras detallaron que GK-1 no causó reacciones adversas en los animales tratados, lo que confirma su seguridad.
En varios casos, el tumor desapareció por completo y, en otras situaciones, se logró prolongar la vida de los animales, según datos publicados por Ciencia UNAM-DGDC.
Sobre su mecanismo de acción, las científicas explican que GK-1 actúa de manera semejante a las inmunoterapias basadas en anticuerpos monoclonales, ya que estimula y dirige la respuesta inmune para destruir las células tumorales.
La molécula también logra inhibir la angiogénesis, es decir, la formación de nuevos vasos sanguíneos que alimentan al tumor y favorecen la propagación de la enfermedad.
Por otro lado, la investigación ha documentado que GK-1 modifica el metabolismo de las células cancerosas al afectar el funcionamiento de sus mitocondrias, debilitando la producción de energía necesaria para su reproducción.
Molécula GK-1 en humanos
Para avanzar hacia el uso clínico, las investigadoras de la UNAM colaboran con el Instituto Nacional de Cancerología (INCan) en el diseño de estudios que permitan evaluar la seguridad del fármaco en humanos.
Actualmente, una empresa en India desarrolla los ensayos de estabilidad del compuesto, cuyos resultados están previstos para 2026.

El grupo también busca financiamiento para llevar a cabo estas pruebas de seguridad, esenciales antes de cualquier aplicación en personas.
En cuanto a su futuro uso, el equipo contempla tanto la aplicación de GK-1 en monoterapia como su combinación con tratamientos ya existentes, con la finalidad de reducir dosis y minimizar toxicidad —aspecto crítico frente a terapias habituales que resultan costosas y agresivas—.
Las científicas expresan su confianza en que la eficacia y seguridad observadas en animales se puedan comprobar en humanos, manteniendo la esperanza de sumar una alternativa real al tratamiento del cáncer de mama triple negativo, según recoge Ciencia UNAM-DGDC.
Más Noticias
Carlos Trejo ‘El Cazafantasmas’ denuncia discriminación en lujoso hotel por su apariencia: llevaba playera de ‘Cañitas’
El investigador paranormal mostró su enojo por un incidente ocurrido en el hotel Safi de Monterrey, donde no se le permitió ingresar por su característico estilo

Resultados Sorteo Mayor 3999 Lotería Nacional hoy 27 de enero 2026: Premio mayor, números ganadores y reintegros
Los premios podrán reclamarse en el edificio de la Lotería Nacional o en los centros de venta autorizados, dentro de un plazo de 60 días a partir de la fecha del anuncio oficial

FGR inició investigación por las narcomantas presuntamente atribuidas al CJNG en Uruapan
Los mensajes colgados en diversos puntos de la ciudad señalan un presunto vínculo entre la administración municipal y delincuentes

México listo para ser sede de cuatro partidos de repechaje para el Mundial, confirman autoridades
Los estadios Akron y BBVA serán el escenario de los juegos de repesca internacional, tras cumplir con mejoras en infraestructura

Pensión Mujeres Bienestar 2026: esta es la fecha límite para recibir pago de 3 mil 100 pesos de este mes de enero
Adultas mayores de 60 a 64 años de edad integran este programa social del Gobierno de México


