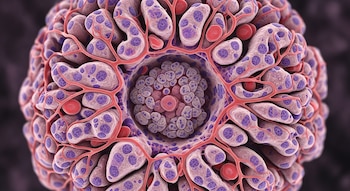
Generar organoides funcionales de múltiples linajes celulares a partir de tejido adiposo humano adulto, sin requerir el aislamiento de células madre ni la manipulación genética del material, representa un avance destacado para la medicina regenerativa.
Según EurekAlert! y ScienceDirect, este método directo simplifica la creación de estructuras biológicas complejas y abre nuevas posibilidades para tratamientos personalizados y accesibles frente a distintas enfermedades.
Las técnicas convencionales para obtener organoides suelen depender del aislamiento y la expansión de células madre, además de procedimientos de manipulación genética. ScienceDirect señala que estos métodos elevan los costes, la dificultad técnica y los riesgos clínicos. Estos procedimientos también presentan limitaciones relacionadas con la escasez de células trasplantables, desafíos éticos y sanitarios, así como el riesgo de aparición de tumores tras el trasplante.
A esto se suma la necesidad de exponer los cultivos celulares a señales bioquímicas precisas y el uso de tecnologías avanzadas de biofabricación, factores que dificultan el uso generalizado de estos organoides en entornos clínicos.
Nueva técnica para transformar tejido adiposo en organoides
Frente a estas restricciones, un equipo de investigación desarrolló una técnica en la que el tejido adiposo humano adulto se transforma directamente en organoides, sin que sea necesario el aislamiento celular tradicional.
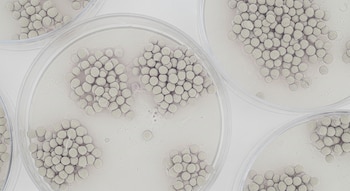
Según EurekAlert!, mediante un sistema de cultivo en suspensión, los investigadores obtuvieron microtejido reagrupado que es capaz de diferenciarse en células procedentes de los tres linajes principales: mesodermo, endodermo y ectodermo. ScienceDirect coincide en que este enfoque es sencillo, seguro y aplicable en un entorno clínico a escala.
Entre los avances logrados, destaca la producción de organoides de médula ósea a partir de microtejido reagrupado, capaces de sostener la hematopoyesis humana. EurekAlert! detalla que, tras ser implantados en ratones inmunodeficientes, estos organoides generaron estructuras óseas con nichos endosteales y perivasculares, facilitando la incorporación y diferenciación de células hematopoyéticas humanas.
ScienceDirect indica que estas estructuras reproducen la organización y función de la médula ósea original, posicionando el método como un referente para estudios en el campo hematológico.
La investigación también exploró aplicaciones en el ámbito endocrino. EurekAlert! señala que, bajo un protocolo de diferenciación en cuatro etapas, los científicos desarrollaron islotes pancreáticos productores de insulina a partir del mismo microtejido reagrupado. Tras su implantación en ratones con diabetes inducida, los organoides mostraron una vascularización rápida y contribuyeron a normalizar los niveles de glucosa en sangre, demostrando así su funcionalidad.
ScienceDirect sugiere que este modelo puede utilizarse tanto para el desarrollo de terapias contra la diabetes como para la experimentación científica.
Formación de tejidos neuronales
El equipo de investigación logró, además, inducir la formación de tejidos neuronales utilizando el microtejido reagrupado. EurekAlert! expone que, bajo condiciones específicas, los pellets de tejido adiposo formaron esferas neurales, que posteriormente se diferenciaron en células con marcadores de neuronas y neuroglía.

ScienceDirect destaca que la plasticidad troncocelular del tejido adiposo adulto desafía las ideas tradicionales sobre la diferenciación celular y amplía las posibles aplicaciones para enfermedades neurológicas y el desarrollo de nuevos modelos experimentales.
Entre las ventajas clínicas, ScienceDirect indica que la estrategia presenta una fuente segura y escalable para terapias regenerativas directamente a partir de tejido adiposo humano. EurekAlert! coincide en que el empleo de microtejido reagrupado reduce la complejidad y los pasos laboriosos que caracterizan a los protocolos convencionales, permitiendo avanzar hacia soluciones más ágiles y económicas, tanto en el desarrollo de tratamientos personalizados como en el modelado de enfermedades.
Las dos fuentes destacan el valor del tejido adiposo humano como alternativa accesible y segura para la generación de organoides, el cual contiene células con capacidad de transdiferenciación, lo que facilita prescindir de fuentes más complejas y técnicas invasivas.
EurekAlert! afirma que el estudio “demuestra el potencial del tejido adiposo humano como recurso para aplicaciones terapéuticas en medicina regenerativa”, mientras que ScienceDirect lo considera una base para ampliar el acceso a nuevas terapias.
A medida que la medicina regenerativa evoluciona, la capacidad de obtener organoides funcionales a partir de tejido adiposo multiplica las opciones para desarrollar terapias más rápidas, seguras y personalizadas para un mayor número de personas.
Últimas Noticias
La ciencia revela el origen de las lágrimas de felicidad y su impacto en la empatía
El reconocimiento del “kama muta” ayuda a comprender por qué, en momentos de conexión profunda, surgen reacciones emocionales intensas que fortalecen la solidaridad y el bienestar, según estudios recientes

Expertos destacan que la calidad de los vínculos sociales es central para la felicidad
Las evidencias científicas recientes destacan la importancia de relaciones humanas auténticas para una vida satisfactoria, mientras que la carencia de conexión social está asociada a riesgos para la salud física y mental, según especialistas

Un sistema automático logra predecir partos prematuros tan rápido como un equipo humano
Un estudio de la Universidad de California mostró que la inteligencia artificial puede acortar los tiempos de validación y publicación en estudios médicos, aunque la supervisión experta sigue siendo clave

Un hallazgo en Níger permite identificar una nueva especie de espinosaurio
La reciente investigación dirigida por Paul Sereno ha aportado detalles sobre un dinosaurio desconocido hasta ahora, cuyas estructuras óseas sugieren una afinidad con aves zancudas y modifican la visión tradicional sobre el género Spinosaurus
La proteína NfL es un nuevo indicador de envejecimiento en animales
Expertos confirman que analizar la sangre y medir dicho neurofilamento ayuda a conocer la salud y la esperanza de vida de muchas especies




