Pese a ser una de las enfermedades parasitarias más letales del mundo, la leishmaniasis visceral sigue siendo prácticamente invisible fuera de zonas empobrecidas de África Oriental, donde afecta a miles de familias cada año. Andrew Ochieng, ex paciente y hoy activista comunitario, recorre las aldeas de Kenia y Uganda sobre su motocicleta, llevando pruebas médicas y motivado por cicatrices físicas y emocionales que arrastra desde su niñez.
Su historia, recogida por la BBC, ilustra cómo la pobreza, el acceso limitado a tratamientos y los arraigos culturales mantienen vigente esta enfermedad, que impacta de manera desproporcionada en la infancia.
A los 12 años, Ochieng sufrió semanas de fiebre intensa y cansancio extremo sin diagnóstico. Sus padres confiaron primero en curanderos tradicionales, quienes realizaron cortes en su abdomen y aplicaron remedios de estiércol y hierbas.
Solo tras varios intentos, logró recibir atención hospitalaria, donde enfrentó un tratamiento de 60 inyecciones en dos meses. Ahora, esas cicatrices impulsan su labor con la Iniciativa de Medicamentos para Enfermedades Olvidadas (DNDi), para evitar que otros niños repitan su experiencia traumática.
Qué es la leishmaniasis visceral y a quién afecta
Unos 600 millones de personas están en riesgo de padecer leishmaniasis visceral, según datos recientes. África Oriental concentra el 73% de los casos globales. Cada año se calculan entre 50.000 y 90.000 nuevos pacientes en todo el mundo, aunque menos de la mitad son registrados oficialmente.
La leishmaniasis visceral, conocida en la región como Kala-azar, es provocada por un parásito transmitido mediante la picadura del flebótomo o mosca de la arena. Es la segunda enfermedad parasitaria más mortal, después de la malaria. Sus síntomas principales son fiebre, pérdida de peso y agrandamiento del hígado y bazo, y sin tratamiento puede provocar la muerte.
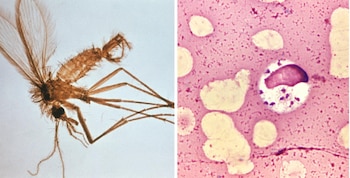
La BBC indica que el 95% de los casos sin atención resultan fatales. Los menores de 15 años representan la mitad de los diagnósticos anuales.
Diagnóstico, síntomas y grupos vulnerables
La identificación temprana puede salvar vidas, pero en la zona los síntomas —dolor articular, fiebre intermitente, hemorragia nasal, inflamación del bazo— suelen ser confundidos o pasados por alto.
Ochieng, hoy movilizador de la DNDi, examina a aldeanos bajo la sombra de acacias en Akorikeya, Uganda, con pruebas rápidas RK39 que arrojan resultados en diez minutos usando una sola gota de sangre.
El peligro aumenta entre quienes viven con VIH, que tienen 100 veces mayor probabilidad de contraer la enfermedad, según explicó Ochieng a la BBC. “De septiembre a febrero, se observan más casos”, advierte el activista, relacionando el alza a la estación seca y la proliferación de flebótomos.
Las condiciones sociales deciden la vida o la muerte. La leishmaniasis visceral aparece donde la pobreza extrema es la norma, las casas carecen de suelo de cemento y los trayectos al hospital más cercano exigen días de caminata. Joy Malongo, gerente de acceso de la DNDi, declaró a la BBC: “La leishmaniasis visceral afecta únicamente a los más pobres entre los pobres”.

El acceso deficiente a la salud y la alimentación, la falta de agua potable y el desplazamiento constante —frecuente entre comunidades como los pokot— perpetúan el contagio. A ello se suman deforestación, nuevos sistemas de riego y cambio climático, que elevan la humedad y temperatura y facilitan los criaderos de flebótomos.
Historias de supervivencia y redes comunitarias
El camino de Ochieng no es una excepción. Chemket Selina, madre de cuatro hijos, recuerda haber padecido malaria y fiebre tifoidea antes de enfrentar la leishmaniasis visceral en su infancia. El diagnóstico solo llegó cuando Ochieng la reconoció y la acompañó unos 20 km hasta el Hospital Amudat.
Selina, como muchas mujeres pokot, enfrenta inseguridad alimentaria y la incertidumbre respecto a la salud de sus hijos. “Lo que encontramos es lo que comemos”, relató a la BBC tras cocinar hojas silvestres como única comida del día. El temor a recaídas y brotes persiste.
La detección activa y el seguimiento comunitario resultan determinantes. Equipos como el de Ochieng visitan hasta 16 aldeas cada mes y rastrean pacientes, incluso frente al reto de familias que migran en busca de agua y pasto.
Tratamiento y desafíos logísticos
El tratamiento estándar en Uganda y Kenia combina estibogluconato de sodio (SSG) y paromomicina durante 17 días, lo que implica 34 inyecciones intramusculares. Los efectos secundarios son serios y pueden afectar el hígado y el corazón. “Es como quimioterapia para el cáncer”, describió la BBC, aludiendo al sufrimiento de los pequeños pacientes bajo mosquiteros en Amudat.
La investigación de la DNDi permitió ensayar nuevas combinaciones, como la miltefosina sumada a paromomicina, que reduce el total de inyecciones y el tiempo de tratamiento, además de graves riesgos. Ambos esquemas superan el 91% de eficacia tras seis meses, pero la combinación sin SSG ofreció mayor seguridad.
Persisten obstáculos logísticos y creencias culturales, como la convicción de que el dolor por las inyecciones es indispensable para la cura.
Hacia la erradicación y el futuro
África Oriental enfrentó brotes recientes, como los de 2020 y 2022 en Kenia, donde casi cuatro millones de personas estuvieron en riesgo elevado. A pesar de los recursos limitados, los trabajadores sanitarios mantienen la esperanza de eliminación.
El doctor Patrick Sagaki destaca el ejemplo de Bangladesh, donde el diagnóstico temprano y la accesibilidad al tratamiento lograron reducir drásticamente los casos. “La eliminación de la leishmaniasis visceral es alcanzable”, defendió el médico, subrayando la importancia de las intervenciones oportunas y la educación comunitaria.
No obstante, mientras persista la pobreza extrema y falten recursos, la amenaza seguirá presente en las mismas familias y comunidades, generación tras generación.
La leishmaniasis visceral en Argentina y América Latina
En América Latina, incluida Argentina, la leishmaniasis visceral presenta características distintas a las observadas en África Oriental. Aunque también se asocia a contextos de vulnerabilidad, la transmisión suele darse en entornos urbanos y periurbanos del noreste del país, donde el flebótomo encuentra condiciones favorables en zonas con vegetación densa, humedad y presencia de animales domésticos, según el Ministerio de Salud de la Nación.

El primer brote urbano relevante en Argentina se detectó en Posadas, Misiones, en 2006, lo que marcó un cambio epidemiológico al evidenciar que la enfermedad podía establecerse en ciudades. Desde entonces, se registraron casos en provincias como Corrientes, Formosa y Chaco.
A diferencia de África, los perros domésticos constituyen el principal reservorio del parásito en la región, lo que convierte a la leishmaniasis canina en un factor clave para la transmisión, de acuerdo con la Organización Panamericana de la Salud (OPS) y el SENASA.
Las estrategias sanitarias incluyen vigilancia epidemiológica, control vectorial, diagnóstico de animales y campañas de prevención para limitar la expansión del flebótomo hacia nuevas áreas favorecida por el cambio climático y la urbanización.
Últimas Noticias
El portaaviones estadounidense Gerald Ford abandonó Grecia y puso rumbo a la costa de Israel
Su partida coincidió con el inicio en Ginebra de una nueva ronda de conversaciones indirectas entre Estados Unidos e Irán sobre el programa nuclear iraní
Xi Jinping continúa su purga militar: el régimen chino expulsa a nueve oficiales de alto rango del Ejército
Una lista compuesta por figuras destacadas fue retirada entre supervisión disciplinaria y nuevas pesquisas internas, justo en la víspera del inicio de la reunión anual para definir políticas importantes hasta 2030 en Beijing
Ucrania y Rusia intercambiaron restos de soldados mientras EEUU sigue intentando avances en las negociaciones
Las autoridades de ambos países llevaron a cabo la repatriación de restos mortales en el contexto del conflicto que se encuentra en su cuarto año

El jefe del OIEA advirtió sobre la incertidumbre nuclear en Irán
Rafael Mariano Grossi expresó que la falta de inspecciones tras el reciente conflicto ha originado vacíos de información, lo que podría incidir significativamente en el rumbo de las negociaciones internacionales en curso
Castillo de Petrelë: del refugio de héroes en la Edad Media al destino favorito de Albania
La fortaleza fue clave en la historia de los Balcanes. Actualmente, combina panorámicas únicas, relatos legendarios y sabores auténticos para viajeros curiosos