
Como suelen decir los expertos en nutrición, algunas grasas son buenas. Pero llevada esta frase al plano de la nueva generación de vacunas que estudian los científicos, significa un posible avance de este material para ganar en eficacia y seguridad de innovadores desarrollos contra varias enfermedades.
Por ejemplo, se pueden citar a las bolitas de grasa que se encuentran en dos de las vacunas contra el COVID-19 más utilizadas en el mundo. Conocidas como nanopartículas lipídicas (LNP), estas pequeñas burbujas de grasa encierran el ARN mensajero (ARNm) que codifica una proteína viral, lo que ayuda a transportarla a las células y protegerla de las enzimas destructivas. Esta tecnología que tenía algunos años, fue perfeccionada en 2020 para el desarrollo y posterior éxito de las vacunas COVID-19 de Moderna y Pfizer-BioNTech. Pero a pesar de lo beneficiosas que son estas grasas, los expertos afirman que todavía hay mucho por mejorar, y que nuevas vacunas podrían ser más eficientes y con menos efectos secundarios al organismo.
PUBLICIDAD
Así, las nanopartículas son una fuente importante de efectos secundarios no deseados cuando se propagan por el cuerpo y desencadenan los dolores y la inflamación que muchas personas experimentan después de la vacunación. Hacen un mal trabajo al descargar su carga una vez dentro de las células, un paso necesario para que la maquinaria de producción de proteínas convierta las secuencias de ARNm en señales de preparación inmunológica. Y debido a que tienden a desmoronarse cuando se calientan, deben almacenarse a bajas temperaturas, lo que limita su uso global.
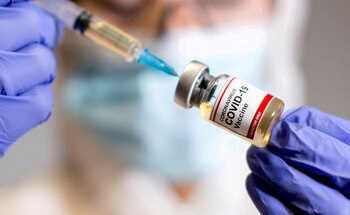
Una nueva generación de LNP con mayor potencia, menos efectos secundarios, mayor estabilidad y propiedades más precisas para dirigirse a los tejidos está ahora en desarrollo en grandes empresas farmacéuticas y de biotecnología. Hay mucho dinero en juego: estas nanopartículas mejoradas podrían conducir a mejores vacunas de ARNm para COVID-19 y otras enfermedades. También podrían ayudar al ARNm a cumplir su promesa como herramienta terapéutica para tratar enfermedades. “Hay innovaciones en la entrega que ciertamente podrían cambiar el juego”, afirmó Philip Santangelo, ingeniero biomédico del Instituto de Tecnología de Georgia que ha colaborado con varias compañías de ARNm.
PUBLICIDAD
El bioquímico Pieter Cullis de la Universidad de Columbia Británica (UBC), Vancouver, junto a colegas, desarrollaron los primeros LNP hace unos 20 años para llevar fármacos silenciadores de genes a las células. Más tarde, él y otros adaptaron los cuatro componentes lipídicos de las LNP para administrar el ARNm que corrige la enfermedad a las células defectuosas. “Ahora que se les está dando un nuevo uso, en las vacunas, todavía hay mucha optimización y desarrollo por hacer”, explicó la bioingeniera de la UBC Anna Blakney, cofundadora de la compañía de vacunas de ARN VaxEquity. Y cuando se trata de comprender cómo las células interactúan con las nanopartículas, “es solo este gran signo de interrogación”, agrega.
Una pista surgió a principios de este año cuando los científicos de Genentech mostraron cómo las nanopartículas activan una vía inflamatoria particular , el eje de la interleucina-1, que es fundamental para generar respuestas inmunitarias protectoras, pero también puede provocar efectos secundarios. Entre los LNP probados, uno hecho con SM-102, un lípido “ionizable” que ayuda a unir y empaquetar el ARNm en LNP, demostró ser un instigador especialmente fuerte de esta vía. Eso podría ayudar a explicar por qué el disparo de Moderna, que se basa en SM-102, es altamente efectivo y propenso a hacer que las personas se sientan repulsivas.
PUBLICIDAD
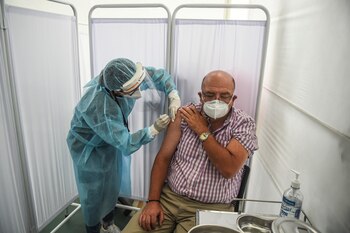
El equipo de Genentech no evaluó el lípido comparable encontrado en la vacuna Pfizer-BioNtech. Pero Mohamad-Gabriel Alameh y sus colegas de la Facultad de Medicina Perelman de la Universidad de Pensilvania probaron uno estrechamente relacionado y descubrieron que desencadenó una amplia gama de moléculas inflamatorias, tanto deseadas como no. “El objetivo ahora es diseñar lípidos ionizables que activen vías inmunitarias favorables sin sobreestimular las perjudiciales”, indicó Alameh, quien cofundó AexeRNA Therapeutics con el bioingeniero Michael Buschmann de la Universidad George Mason y otros. “¿Es muy sencillo? No”, dice Alameh, pero debería ser posible.
Antes de su muerte en marzo, Buschmann lideró un equipo que en 2021 demostró cómo la carga eléctrica de las LNP es fundamental para el éxito de la vacuna . Una carga negativa hace que sea menos probable que la partícula permanezca en el músculo y los ganglios linfáticos de los ratones inyectados, donde podría provocar respuestas inmunitarias beneficiosas; en cambio, tiende a propagarse ampliamente, lo que aumenta el riesgo de fiebre, escalofríos y otras reacciones adversas.
PUBLICIDAD
Para hacer una nanopartícula con menos carga negativa, los investigadores modificaron la química del lípido ionizable. Cuando se formuló en una vacuna de ARNm para COVID-19, el nuevo portador de LNP incitó a los ratones a producir más anticuerpos protectores que los sistemas de administración estándar y tuvo menos efectos secundarios, según los datos publicados el año pasado en forma de preimpresión y ahora bajo revisión en Nature Communications.

Dan Peer, bioquímico de la Universidad de Tel Aviv y cofundador de la startup de administración de vacunas NeoVac, también ha desarrollado bibliotecas de nuevos lípidos ionizables con estructuras atípicas. En experimentos no publicados, parecen permitir mejores vacunas de ARNm con menos efectos secundarios y también extienden su estabilidad en almacenamiento a temperatura ambiente. Otras mejoras podrían provenir de impulsar la absorción de LNP en las células y luego mejorar su capacidad para liberarse de los sacos de la membrana celular, conocidos como endosomas, que los transportan al interior. La gran mayoría de los LNP quedan atrapados en estos receptáculos y luego se destruyen o expulsan sin entregar sus cargas útiles de vacunas, lo que significa que “hay una gran cantidad de ARN que no se está utilizando”, dice Gaurav Sahay, bioingeniero de la Universidad de Ciencias y Salud de Oregón.
PUBLICIDAD
La forma de los lípidos ionizables afecta la capacidad de un LNP para alterar un endosoma, al igual que el colesterol, una de las otras grasas en los LNP. Junto con los científicos de Moderna, Sahay y sus colegas informaron en 2020 que el uso de diferentes formas de colesterol puede mejorar las tasas de escape de LNP del atrapamiento endosómico . Ha fundado una empresa llamada Enterx Biosciences para comercializar sus descubrimientos.
Sanofi ha comenzado a evaluar algunos de sus LNP personalizados en ensayos con humanos. En un estudio lanzado en 2021, por ejemplo, la compañía evaluó dos opciones de LNP para administrar una vacuna contra la gripe de ARNm que está desarrollando. Según datos preliminares, una formulación de lípidos demostró ser mucho mejor para impulsar la inmunidad contra la influenza , anunció Frank DeRosa, jefe de investigación y biomarcadores en el Centro de excelencia de ARNm de Sanofi, en un evento para inversores en diciembre de 2021. Pero el mismo LNP también provocó Efectos secundarios más frecuentes a dosis más altas.
PUBLICIDAD

Otras empresas, incluidas BioNTech y Arcturus Therapeutics, han comenzado a explorar formas de eliminar el polietilenglicol, un compuesto que ayuda a estabilizar las LNP, pero que también se ha relacionado con algunos tipos de malas reacciones a las vacunas. Mientras tanto, muchas más empresas se centran en optimizar los lípidos para entregar ARNm para tratar enfermedades en lugar de prevenirlas. Esto requiere llevar ARNm que codifiquen proteínas correctoras de enfermedades a las células y tejidos precisos donde se necesitan, no solo al hígado, donde las formulaciones actuales de LNP tienden a terminar después de la infusión.
“La entrega de LNP será clave para expandir realmente el alcance del ARNm” más allá de las vacunas preventivas, dice Dominik Witzigmann, cofundador y director ejecutivo de la empresa emergente NanoVation Therapeutics, fundada por Cullis.
PUBLICIDAD
SEGUIR LEYENDO:
PUBLICIDAD
PUBLICIDAD
PUBLICIDAD
Últimas Noticias
Descubren una nueva pista genética sobre una enfermedad que afecta el sistema nervioso y el corazón
Un equipo de la Universidad de Pensilvania, en Estados Unidos, identificó que el “silenciamiento” de un gen puede agravar el cuadro de ataxia de Friedreich

Detectives del espacio: la NASA convoca al público para descifrar el fenómeno que amenaza al GPS y las redes eléctricas
La agencia estadounidense lanza Shock Detectives, un proyecto abierto que busca entender mejor la interacción entre el viento solar y el campo magnético terrestre a través de la colaboración ciudadana

Mundial 2026: cuáles son las vacunas que se deben aplicar para viajar seguro
El auge de casos de sarampión en Estados Unidos, Canadá y México alertan a las autoridades sanitarias frente a la llegada de millones de turistas. Las otras vacunas clave necesarias para evitar brotes
Cómo las tormentas en la Tierra alteran el clima espacial: los datos de una misión de la NASA
La agencia apagó el instrumento instalado en el exterior de la Estación Espacial Internacional el 21 de mayo, tras 30 meses de observaciones infrarrojas

La cantidad de personas con trastornos mentales se duplicó desde 1990, reveló un estudio en The Lancet
Las afecciones psiquiátricas ya superan a las enfermedades cardiovasculares como principal causa de discapacidad mundial. Desde la pandemia, muestran subas asociadas a ansiedad y depresión. A quiénes afectan más



