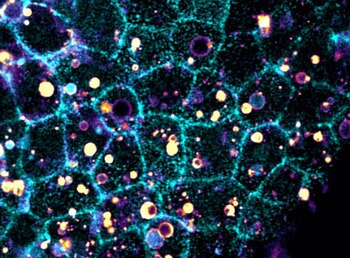
En tejidos de modelos animales como peces cebra y ratones, la observación directa mediante filmaciones permitió identificar que las células vivas despliegan una labor activa al descomponer y fragmentar células defectuosas antes de eliminarlas por completo. El medio CSIC detalló que este mecanismo, captado en video, implica que las células sanas rodean y “muerden” a las células muertas o dañadas, facilitando así su ingestión, lo que representa un cambio de paradigma respecto a la comprensión previa sobre cómo el organismo evita la acumulación celular que puede derivar en inflamación y diversas patologías asociadas.
De acuerdo con el CSIC, el estudio liderado por Esteban Hoijman, del Instituto de Biología Molecular de Barcelona (IBMB-CSIC) y del Instituto de Investigación Biomédica de Bellvitge (IDIBELL), junto con Ivan K. H. Poon, de la Universidad La Trobe de Australia, aportó evidencia in vivo sobre el comportamiento de las células en organismos animales. El equipo aprovechó modelos vivos para documentar por primera vez el proceso mediante el cual, dentro del tejido, las células sanas ejecutan una función dual: fragmentan los restos celulares para, acto seguido, engullirlos y eliminarlos.
Según publicó el CSIC, hasta el momento la mayor parte de los conocimientos sobre la eliminación celular derivaban de estudios realizados en cultivo, lo que limitaba la comprensión real del proceso en organismos completos. En esas condiciones, se suponía que era la célula defectuosa la responsable de su propia fragmentación antes de ser ingerida, a través del proceso de apoptosis. Sin embargo, la evidencia visual obtenida en este nuevo estudio reveló que la iniciativa parte de las células vivas circundantes, quienes fragmentan activamente la célula objetivo, lo que permite que células de tamaño similar puedan luego ser eliminadas eficientemente.
Durante la fagocitosis, según reportó el CSIC, la célula encargada de limpiar los tejidos se enfrenta al desafío de que su objetivo posee dimensiones comparables a las propias. Por eso el desglose en fragmentos más pequeños se vuelve crucial para garantizar que la ingestión y posterior destrucción se lleven a cabo sin problemas. Esta mecánica se aprecia claramente gracias a las imágenes captadas durante el estudio.
Esteban Hoijman explicó en declaraciones al CSIC que “las células que fagocitan mastican a las que van a ingerir, es decir, las rompen en partes más pequeñas para facilitar su ingestión. Este proceso es similar al que ocurre en nuestras bocas al masticar la comida, pero a nivel microscópico”. El informe del CSIC indica que las células encargadas de fagocitar emplean extensiones de su membrana para fragmentar los restos celulares, desarrollando una actividad comparable a la masticación en el contexto de los tejidos vivos.
El proceso de destrucción eficiente de restos celulares influye directamente en la prevención de enfermedades inflamatorias, según expuso el CSIC. La acumulación de fragmentos celulares en órganos como el intestino, los pulmones y las articulaciones puede inducir procesos inflamatorios vinculados a afecciones como la colitis, la artritis o diferentes formas de alergias respiratorias. Además, la desregulación de la apoptosis, el mecanismo por el cual una célula determina su eliminación, se relaciona con la aparición de cánceres y patologías neurodegenerativas, según consignó Science Advances, medio en el que se publicó la investigación.
El CSIC destaca que el hallazgo tiene relevancia potencial para el desarrollo de terapias destinadas a mejorar la función fagocítica en situaciones donde los residuos celulares se acumulan y contribuyen al deterioro tisular o a la enfermedad. Los investigadores consideran que este conocimiento abre la puerta a futuras intervenciones clínicas enfocadas no solo en el tratamiento de la inflamación, sino también en la prevención de enfermedades cuyo origen se asocia a la acumulación inepta de células muertas o defectuosas.
A lo largo de la investigación, el equipo observó que la eliminación activa de células muertas es esencial tanto en organismos adultos como en etapas embrionarias. El CSIC detalló que este proceso biológico esencial sostiene la homeostasis y protege los tejidos frente a la inflamación crónica, subrayando el valor de observar fenómenos celulares directamente en tejidos vivos. La información obtenida permite conocer con mayor precisión cómo las células mantienen el equilibrio al eliminar residuos a ritmos adecuados y en cooperación con sus vecinas.
El CSIC informó que millones de células mueren diariamente en los organismos, ya sea por renovación natural o debido a defectos que impiden su funcionamiento. El correcto reciclaje y eliminación previene la activación de vías inflamatorias. Cuando la acumulación de restos se prolonga, el riesgo de mecanismos inflamatorios persistentes y la progresión hacia enfermedad resulta elevado.
Estudios previos trasladaban las conclusiones de sistemas simplificados de cultivo a la biología real de los tejidos, pero esta investigación —dirigida por Hoijman y Poon— demuestra la necesidad de analizar estos procesos en condiciones orgánicas vivas. Gracias a ello, los investigadores citados por el CSIC avanzan en la descripción de las estrategias celulares de cooperación y fragmentación que anticipan la ingestión de residuos, lo que a su vez permite un mayor entendimiento de los mecanismos que sostienen la salud de los tejidos y la estabilidad del ambiente celular.
Finalmente, el equipo investigador, según reportó el CSIC, plantea como línea prioritaria continuar explorando y caracterizando los mecanismos celulares implicados en la fragmentación y eliminación de células defectuosas. Estos trabajos podrán orientar el desarrollo de opciones terapéuticas capaces de reforzar la capacidad del cuerpo para reciclar y gestionar su propia carga celular, con miras a controlar o prevenir enfermedades donde el acopio anómalo de restos celulares conlleva consecuencias patológicas.
Últimas Noticias
EEUU autoriza a India a comprar petróleo ruso durante un mes por el conflicto en el golfo Pérsico
Washington concede a Nueva Delhi una exención que le permite abastecerse de crudo ruso durante 30 días, en plena crisis energética provocada por el reciente bloqueo iraní al estrecho de Ormuz y la escalada de tensiones en Oriente Medio

La Justicia ratifica la prisión permanente para el 'El Portugués' por el atropello mortal en una boda de Torrejón
Los magistrados madrileños desestiman los recursos y confirman la condena máxima para Micael da Silva, acusado de arrollar a varios asistentes durante una celebración, tras considerar que actuó de forma plenamente consciente de sus actos

Dimiten los tres consejeros de GIP (BlackRock) en Naturgy tras salir el fondo de su accionariado
Tras la venta del 11,4% de las acciones por parte de GIP, Lucy Chadwick, Rajaram Rao y Martin Catchpole renuncian a su cargo como representantes, cerrando así una etapa de diez años dentro del consejo de administración de la energética

Italia cierra su Embajada en Irán "por motivos de seguridad" en medio de la ofensiva de EEUU e Israel
Unos 50 ciudadanos italianos, incluido el embajador, fueron evacuados hacia Azerbaiyán tras el retiro diplomático, mientras la crisis en Oriente Próximo deja más de 1.200 fallecidos y provoca represalias iraníes en toda la región

Iberdrola completa la compra de su primer parque eólico en el estado de Victoria (Australia)

