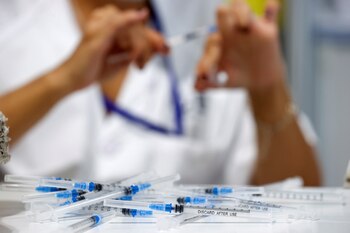
La Haya, 2 dic (EFE).- La Agencia Europea de Medicamentos (EMA) comenzó este jueves a evaluar en tiempo real los datos emergentes de la vacuna de virus inactivado conocida como VLA2001, desarrollada por la farmacéutica francesa Valneva, que se convierte en el quinto preparado contra la covid-19 que está analizando este regulador de fármacos.
El comité de medicamentos de uso humano (CHMP) ha iniciado un proceso de “revisión continua” de esta vacuna en base a los resultados preliminares de los estudios de laboratorio y los primeros estudios clínicos en adultos que sugieren que desencadena la producción de anticuerpos que atacan el SARS-CoV-2, el virus que provoca la covid-19.
Este proceso de análisis significa que la agencia irá evaluando los datos a medida que vayan estando disponibles hasta reunir la suficiente información para decidir si los beneficios de su aprobación y uso contra la covid-19 superan los riesgos de sus posibles efectos secundarios.
La revisión continuará hasta que haya suficientes evidencias disponibles para que la farmacéutica dé el paso de solicitar formalmente una licencia europea para el uso de su vacuna en todos los países de la Unión Europea (UE) con el respaldo de los expertos de la EMA, lo que puede tardar unos meses en llegar.
“La Agencia evaluará el cumplimiento de VLA2001 con las normas habituales de la UE en cuanto a eficacia, seguridad y calidad. Si bien EMA no puede predecir los plazos generales, debería llevar menos tiempo de lo normal evaluar una eventual solicitud (de la licencia) debido al trabajo adelantado durante la revisión continua”, explica la agencia.
El calendario de aprobación estará más claro cuando la farmacéutica solicite la autorización de comercialización de la vacuna en la UE.
Esta vacuna prepara al cuerpo para defenderse del contagio con el SARS-CoV-2 con la tecnología de virus inactivado (que no puede provocar la enfermedad) usada en las vacunas tradicionales, que han sido utilizadas de forma segura y eficaz desde mediados del pasado siglo, por ejemplo, en las vacunas de la gripe.
Esta vacuna contiene también dos "adyuvantes", una sustancia que ayuda a fortalecer la respuesta inmunológica a un antígeno. Cuando una persona recibe la inyección, su sistema inmunológico identifica el virus inactivado como "extraño" y produce anticuerpos contra él, preparándolo para futuros contactos con el coronavirus.
La Comisión Europea (CE) aprobó el pasado 10 de noviembre un contrato con la farmacéutica Valneva para adquirir el año que viene 27 millones de dosis de su vacuna contra la Covid-19 y tener derecho a comprar otros 33 millones adicionales en 2023, siempre que la empresa logre el visto bueno de la EMA.
Hay otras tres vacunas que se encuentran en la fase de evaluación continua en el CHMP: la rusa Sputnik V, la china Vero Cell y la francesa Vidprevty.
En una fase más avanzada, porque ya solicitó el respaldo de la EMA a su licencia, está la vacuna estadounidense Novavax, que “se podría aprobar en cuestión de semanas”, según anunció la directora ejecutiva de la EMA, Emer Cooke, el pasado martes. EFE
ir/cat/pi
(Más información sobre la Unión Europea en euroefe.euractiv.es)
Últimas Noticias
Rusia derriba 80 drones ucranianos sobre ocho regiones rusas y los mares Negro y Azov

El brent sube más del 7 % en la apertura de bolsa de Madrid y ronda 100 dólares por barril

El Nikkei cae un 1,04 % tras repunte de precio del petróleo pese a medidas para contenerlo

La nueva ansiedad digital: 8 de cada 10 españoles temen que alguien mire la pantalla de su móvil en espacios públicos
El incremento del uso de teléfonos inteligentes en lugares concurridos ha elevado la preocupación por la privacidad visual, según Ipsos y Samsung, ante el temor de que personas cercanas accedan a información sensible mientras se manipulan dispositivos digitales
China aprueba su nuevo plan quinquenal, con foco en consumo y autosuficiencia tecnológica

