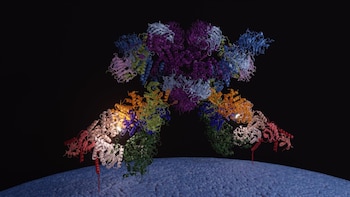
La resolución de la estructura del complejo SEA, encargado de regular a la proteína TOR, ha permitido detectar cambios radicales en la forma en que las células perciben y procesan la información sobre la abundancia de nutrientes, según recoge el medio Nature Structural & Molecular Biology. Este hallazgo, encabezado por Lucas Tafur en el Centro Nacional de Investigaciones Oncológicas (CNIO), ofrece perspectivas sobre los mecanismos que subyacen a patologías como el cáncer y potenciales vías para desarrollar terapias de intervención más específicas.
Las células utilizan diferentes mecanismos para detectar la presencia de nutrientes, y esos mecanismos terminan influyendo en el crecimiento celular. De acuerdo con los datos publicados por Nature Structural & Molecular Biology y difundidos por CNIO, la proteína TOR —en mamíferos denominada mTOR— actúa como uno de los principales sensores para decidir si existen recursos suficientes para que las células crezcan o, por el contrario, deban ahorrar energía. Según detalló Tafur a dicho medio, "Cuando faltan nutrientes, TOR se inhibe y la célula frena el crecimiento, y cuando hay muchos recursos, como aminoácidos o glucosa, pasa al contrario: TOR se activa y promueve el crecimiento celular y la proliferación".
PUBLICIDAD
El funcionamiento preciso de TOR se encuentra en el núcleo de este proceso. Tal como publicó Nature Structural & Molecular Biology, la proteína opera como parte de dos grandes complejos moleculares, TORC1 y TORC2, integrados por varias proteínas ensambladas. La regulación sobre cómo y cuándo activa o detiene el crecimiento se produce a través de otros complejos de proteínas, y no de forma directa por los nutrientes. Lucas Tafur, responsable del Grupo de Mecanismos Estructurales del Crecimiento Celular del CNIO, subrayó la importancia de conocer con detalle esa maquinaria para poder identificar oportunidades que permitan una intervención farmacológica más selectiva y con menos efectos secundarios. "Un fármaco que interfiera con la actividad total de TOR tiene muchos efectos secundarios. Pero si entendemos en detalle la maquinaria que regula a TOR, podemos encontrar la manera de intervenir más selectivamente", explicó el investigador al medio científico.
La investigación dirigida por Tafur se apoya en el estudio de la levadura 'Saccharomyces cerevisiae'. De acuerdo con lo consignado en Nature Structural & Molecular Biology, las similitudes estructurales y funcionales entre la TOR de la levadura y la de los humanos facilitan la extrapolación de descubrimientos entre ambos sistemas biológicos. TOR no solo está presente en seres humanos y hongos, sino que ha sido conservado a lo largo de la evolución en organismos tan diversos como primates, aves, insectos, peces e incluso plantas, desempeñando una función esencial en la evaluación de la disponibilidad de nutrientes para el crecimiento celular.
PUBLICIDAD
Informó Nature Structural & Molecular Biology que la proteína fue bautizada como TOR por ser el “Target of Rapamycin”, en referencia a la rapamicina, una molécula extraída originalmente de suelos de la Isla de Pascua en 1975. La rapamicina, por sus propiedades inmunosupresoras y anticancerígenas, ya formaba parte de tratamientos médicos, especialmente en el contexto de trasplantes, antes de que se identificara su relación con TOR en la década de 1990 tras investigaciones con levadura. Estos antecedentes han colocado a TOR en el centro de la investigación biomédica mundial.
Desentrañar el funcionamiento de TOR implica determinar la estructura de complejos proteicos cuya organización y forma continúan siendo un reto, explica el medio científico. Para abordar este desafío, el equipo de Tafur ha empleado la crio-microscopía electrónica, técnica que congela las muestras a -196℃ —la temperatura del nitrógeno líquido— para obtener imágenes tridimensionales a resolución casi atómica de los componentes moleculares. Mediante este procedimiento, Tafur y sus colaboradores han resuelto la estructura del complejo SEA, también denominado GATOR.
PUBLICIDAD
El complejo SEA, de acuerdo con lo publicado en Nature Structural & Molecular Biology, se describe como un “gran regulador” de TOR capaz de integrar señales diversas relacionadas con los nutrientes, como los aminoácidos, el colesterol y la glucosa. Aunque se conocía su papel crucial, la forma en que integra esas señales no se comprendía del todo. El artículo señala que, contra lo que postulaban teorías anteriores, la propia arquitectura de SEA no presenta dos partes cuyo funcionamiento se regula mutuamente, sino que actúa de manera conjunta. “Vemos que ese concepto no es completamente cierto, no hay una subdivisión dentro del complejo de forma que una parte bloquea a la otra, sino que funciona como un todo”, declaró Tafur al medio.
Otro de los hallazgos destacados consiste en que una sola mutación en un aminoácido basta para alterar completamente el sistema de activación o inhibición de TOR. Según explica Tafur en Nature Structural & Molecular Biology, “Esta actividad es como un interruptor, que no solamente se necesita —como siempre se ha pensado— para inhibir a TOR, sino que también se necesita para activarlo rápidamente”. Este descubrimiento ayuda a explicar el origen de ciertas enfermedades, incluida la aparición de tumores cuando falla este sistema, y sugiere que sería factible modular la acción de TOR de manera selectiva para minimizar los efectos adversos en tratamientos futuros.
PUBLICIDAD
El trabajo de Tafur, según narra el medio científico, no solo aporta conocimientos sobre el engranaje molecular sino que abre la puerta a estrategias terapéuticas innovadoras en patologías vinculadas al metabolismo y al crecimiento celular. Tanto la versatilidad evolutiva de TOR como la posibilidad de intervenir en puntos específicos del sistema reafirman su relevancia en la biología celular y médica.
Últimas Noticias
El Gobierno incrementa en 7 millones las ayudas al cine hasta alcanzar los 62 millones para producción de largometrajes

Moreno afirma que el debate de RTVE mostró el "lío" de los otros candidatos y la "mentira interiorizada" en Montero

El cortometraje sobre sinhogarismo en España de Richard Gere se proyectará en el Foro Urbano Mundial de ONU-Hábitat

EEUU afirma que el alto el fuego con Irán se mantiene a pesar de los ataques en Ormuz

El Gran Fondo Ézaro 2026 se traslada al 3 de octubre por la presión turística

