
Frente a la actual pandemia por coronavirus, se están desarrollando más de 160 vacunas contra el SARS-CoV-2 en todo el mundo, que produce la enfermedad COVID-19, con la esperanza de llevar una al mercado en un tiempo récord para aliviar la crisis mundial.
Se están realizando varios esfuerzos para ayudar a que eso sea posible, incluida la iniciativa Operation Warp Speed del gobierno de EEUU, que ha prometido 10 mil millones de dólares de aporte, con el objetivo de desarrollar y entregar 300 millones de dosis de una vacuna segura y efectiva contra el coronavirus para enero de 2021.
PUBLICIDAD

La Organización Mundial de la Salud (OMS) también busca coordinar los esfuerzos mundiales para desarrollar una vacuna, con miras a entregar 2000 millones de dosis para fines de 2021.
Los candidatos, como todas las vacunas, esencialmente apuntan a instruir al sistema inmunitario para que monte una defensa, que a veces es más fuerte de lo que se proporcionaría a través de una infección natural y tiene menos consecuencias para la salud.
PUBLICIDAD
Para hacerlo, algunas vacunas usan el coronavirus completo, pero en estado muerto o debilitado. Otros usan solo una parte del virus, ya sea una proteína o un fragmento. Algunos transfieren las proteínas del coronavirus a un virus diferente que es poco probable que cause la enfermedad o que incluso sea incapaz de contraerla.

Finalmente, algunas vacunas en desarrollo dependen del despliegue de piezas del material genético del coronavirus, por lo que nuestras células pueden producir temporalmente las proteínas del coronavirus necesarias para estimular nuestro sistema inmunológico. (Esto es lo que son las vacunas y cómo funcionan).
PUBLICIDAD
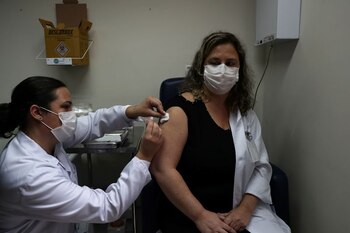
Por lo general, puede llevar de 10 a 15 años llevar una vacuna al mercado. La más rápida, la vacuna contra las paperas, requirió 4 años en la década de 1960. Las vacunas pasan por un proceso de ensayo clínico de varias etapas, que comienza con la fase 1 en donde se busca verificar su seguridad y si desencadenan una respuesta inmune en un pequeño grupo de humanos sanos.
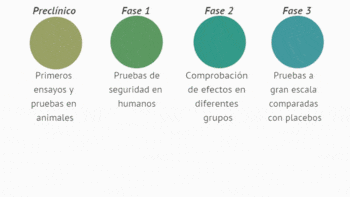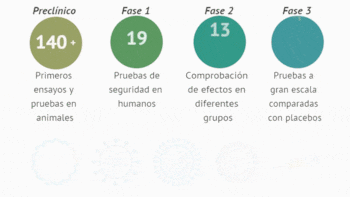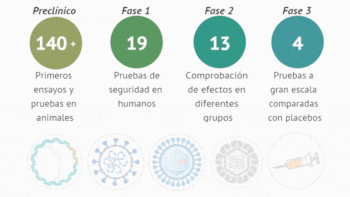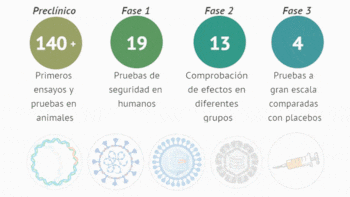
La segunda fase amplía el grupo de pruebas para incluir grupos de personas que pueden tener la enfermedad o tienen más probabilidades de contraerla, para medir la efectividad de la vacuna. La tercera fase amplía el grupo hasta miles para garantizar que la vacuna sea segura y efectiva entre una gama más amplia de personas, dado que la respuesta inmune puede variar según la edad, el origen étnico o las condiciones de salud subyacentes. Luego, las agencias reguladoras de cada país realizan los análisis pertinentes para su aprobación final, lo que puede ser un proceso largo en sí mismo, si es que no se participa directamente de un ensayo clínico previamente.
PUBLICIDAD
Incluso después de que se aprueba una vacuna, se enfrentan obstáculos potenciales en lo que respecta a la fabricación y distribución: desde aumentar la producción para satisfacer las demandas hasta decidir qué poblaciones deben obtenerla primero y a qué costo.
Muchas vacunas también permanecen en la llamada fase cuatro, una etapa perpetua de estudio regular. Pero los desarrolladores de vacunas están tratando de comprimir ese proceso para SARS-CoV-2 ejecutando fases de ensayos clínicos simultáneamente, y la Administración de Drogas y Alimentos de los Estados Unidos (FDA, por sus siglas en inglés), ha prometido acelerar esta traza en el proceso de aprobación.
PUBLICIDAD
Aunque es demasiado pronto para decir qué candidatos serán finalmente exitosos, aquí hay un vistazo rápido a las perspectivas de la vacuna que han llegado a la fase tres y más allá, incluida una introducción rápida sobre cómo funcionan y dónde se encuentran.
Terapéutica Moderna
PUBLICIDAD

Nombre: ARNm-1273
Quién: Una empresa de biotecnología con sede en Massachusetts, en colaboración con los Institutos Nacionales de Salud (NHI).
PUBLICIDAD
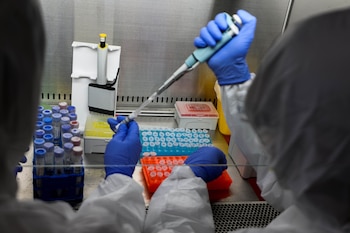
Qué: Esta vacuna candidata se basa en inyectar fragmentos de material genético de un virus, en este caso ARNm, en las células humanas. Crean proteínas virales que imitan el coronavirus, entrenando al sistema inmune para que reconozca su presencia. Esta tecnología nunca ha sido autorizada para ninguna enfermedad. Si tiene éxito, sería la primera vacuna de ARNm aprobada para uso humano.
Estado: El 27 de julio, Moderna anunció que había comenzado la tercera fase de sus ensayos clínicos, incluso mientras continúa monitoreando los resultados de la fase dos. Los resultados preliminares de la fase uno, han demostrado que los sujetos sanos produjeron anticuerpos contra el coronavirus y una reacción de las células T, otro brazo de la respuesta inmune humana. La fase tres probará la vacuna en 30.000 participantes de EEUU. Moderna dice que está en camino de entregar al menos 500 millones de dosis por año a partir de 2021, gracias en parte al acuerdo que ha alcanzado con el fabricante suizo Lonza que le permitirá fabricar hasta 1000 millones de dosis.
PUBLICIDAD
Pfizer

Nombre: BNT162b2
Quién: Es la compañía farmacéutica más grandes del mundo, con sede en Nueva York, en colaboración con la empresa alemana de biotecnología BioNTech.
Qué: Pfizer y BioNTech también están desarrollando una vacuna de ARNm basada en los esfuerzos anteriores de la compañía alemana para utilizar la tecnología en vacunas experimentales contra el cáncer. Pfizer ha firmado un contrato de casi 2 mil millones de dólares con el gobierno de los EEUU. Busca llegar a las 100 millones de dosis para diciembre de 2020, un hecho que entrará en vigencia cuando el medicamento sea aprobado y entregado.
Estado: el 27 de julio, Pfizer y BioNTech lanzaron una prueba que combina las fases dos y tres al inscribir a una población diversa en áreas con transmisión significativa de SARS-CoV-2. Examinará el efecto de la vacuna en 30.000 personas de 39 estados de EEUU, en Brasil, Argentina y Alemania. El proyecto tiene como objetivo buscar una revisión regulatoria tan pronto como octubre de 2020 para cumplir con la fecha límite de diciembre, y espera suministrar 1300 millones de dosis para fines de 2021. Los resultados preliminares de los datos de la fase uno / dos muestran que la vacuna produce anticuerpos y respuestas de células T específico para la proteína SARS-CoV-2.
Universidad de Oxford

Nombre: ChAdOx1 nCoV-19
Quién: La universidad del Reino Unido, en colaboración con la empresa biofarmacéutica AstraZeneca.
Qué: el candidato de Oxford es lo que se conoce como una vacuna de vector viral, esencialmente un “caballo de Troya” presentado al sistema inmune. El equipo de investigación de Oxford transfirió la proteína de la punta del SARS-CoV-2, que ayuda al coronavirus a invadir las células, a una versión debilitada de un adenovirus, que generalmente causa el resfriado común. Cuando este adenovirus se inyecta en humanos, la esperanza es que la proteína espiga desencadene una respuesta inmune. AstraZeneca y Oxford planean producir mil millones de dosis de vacuna que acordaron vender al costo.
Estado: los resultados preliminares de las primeras dos fases de ensayos clínicos de este candidato revelaron que la vacuna había desencadenado una fuerte respuesta inmune, incluido un aumento de los anticuerpos y las respuestas de las células T, con solo efectos secundarios menores, como fatiga y dolor de cabeza. Ahora ha pasado a la fase tres de ensayos clínicos, con el objetivo de reclutar hasta 50.000 voluntarios en Brasil, el Reino Unido, los Estados Unidos y Sudáfrica.
Sinovac

Nombre: CoronaVac
Quién: Una compañía biofarmacéutica china, en colaboración con el centro de investigación brasileño Butantan.
Qué: CoronaVac es una vacuna inactivada, lo que significa que utiliza una versión no infecciosa del coronavirus. Si bien los agentes patógenos inactivados ya no pueden producir enfermedades, aún pueden provocar una respuesta inmune, como con la vacuna anual contra la influenza.
Estado: el 3 de julio, la agencia reguladora de Brasil otorgó la aprobación de esta vacuna candidata para avanzar a la fase tres, ya que continúa monitoreando los resultados de los ensayos clínicos de fase dos. Sinovac dice que las primeras fases han demostrado hasta ahora que la vacuna produce una respuesta inmune sin efectos adversos graves. Los resultados preliminares de las pruebas anteriores de este candidato en monos macacos, publicados en Science, revelaron que la vacuna produjo anticuerpos que neutralizaron 10 cepas de SARS-CoV-2. La fase tres reclutará a casi 9000 profesionales de la salud en Brasil.
Sinopharm

Nombre: ninguno
Quién: la compañía farmacéutica estatal de China, en colaboración con el Instituto de Productos Biológicos Wuhan.
Qué: Sinopharm también está utilizando una vacuna inactivada de SARS-CoV-2 que espera llegue al público a fines de 2020. Sinopharm ha informado que los primeros ensayos de su candidato a vacuna desencadenaron una fuerte respuesta de anticuerpos neutralizantes en los participantes, sin efectos adversos graves. efectos
Estado: a mediados de julio, Sinopharm lanzó su ensayo de fase tres entre 15.000 voluntarios, de 18 a 60 años, sin condiciones subyacentes graves, en los Emiratos Árabes Unidos. La compañía seleccionó los EAU, ya que tiene una población diversa con aproximadamente 200 nacionalidades diferentes, por lo que es un campo de pruebas ideal.
Instituto de Investigación Infantil Murdoch
Nombre: ensayo BRACE Bacillus Calmette-Guerin
Quién: El instituto de investigación en salud infantil más grande de Australia, en colaboración con la Universidad de Melbourne.
Qué: Durante casi cien años, la vacuna Bacillus Calmette-Guerin (BCG) se ha utilizado para prevenir la tuberculosis al exponer a los pacientes a una pequeña dosis de bacterias vivas. A lo largo de los años, ha surgido evidencia de que esta vacuna puede estimular el sistema inmunológico y ayudar al cuerpo a combatir otras enfermedades también. Los científicos están investigando si estos beneficios también pueden extenderse al SARS-CoV-2, y este ensayo ha alcanzado la fase tres en Australia.
Estado: en abril, investigadores del Instituto de Investigación de Niños Murdoch comenzaron una serie de ensayos controlados aleatorios que evaluarán si BCG también podría funcionar en el coronavirus. Su objetivo es reclutar a 10.000 trabajadores de la salud en el estudio.
CanSino Biologics

Nombre: Ad5-nCoV
Quién: una empresa biofarmacéutica china.
Qué: CanSino ha desarrollado una vacuna de vector viral, utilizando una versión debilitada del adenovirus como vehículo para introducir la proteína de la punta del SARS-CoV-2 en el cuerpo. Los resultados preliminares de los ensayos de fase dos, publicados en The Lancet, han demostrado que la vacuna produce “respuestas inmunes significativas en la mayoría de los receptores después de una única inmunización”. No se documentaron reacciones adversas graves.
Estado: aunque la compañía todavía está técnicamente en la fase dos de su prueba, el 25 de junio, CanSino se convirtió en la primera compañía en recibir una aprobación limitada para usar su vacuna en personas. El gobierno chino ha aprobado la vacuna solo para uso militar, por un período de un año.
SEGUÍ LEYENDO:
PUBLICIDAD
PUBLICIDAD
Últimas Noticias
Los nuevos 60: los cambios en la dieta adulta que pueden agregar casi 10 años de vida
Los cambios en la dieta en la edad adulta pueden agregar casi 10 años de vida según un amplio estudio científico. Una guía de pequeños grandes hábitos para alcanzar la plenitud

9 tips para comenzar a hacer deporte y mejorar el estado físico
Una guía para evitar las excusas y ponerse en movimiento. Incorporar desafíos de manera paulatina y armar una rutina son los pasos claves para empezar

Día Mundial del Pene: cuidados para la higiene adecuada y consejos para prevenir el cáncer y otras enfermedades
La fecha busca celebrar la fertilidad y generar conciencia acerca de la práctica del sexo seguro. La salud y el cuidado del órgano reproductor masculino son fundamentales para mantener una vida sexual plena y saludable

Turbulencias durante el vuelo: cinco consejos para subirse al avión sin miedo
Un piloto comercial explica por qué son habituales estos movimientos, además brindó recomendaciones sobre qué asiento elegir para sufrir menos durante el viaje. Una guía práctica y sencilla sobre algunos de los puntos más consultados por los pasajeros

Cuáles son los tres desayunos ideales para personas con diabetes e hipertensión
Las clásicas tostadas con mermelada pueden reemplazarse por opciones más saludables, con más proteínas, fibras y minerales. Cómo ayudan a controlar estas enfermedades




