Come è successo mesi fa in diversi paesi del mondo, il 4 gennaio, la National Administration of Drugs, Food and Medical Technology ( ANMAT) ha approvato l'uso individuale di quattro test di autovalutazione basati sul rilevamento del virus SARS-CoV-2.
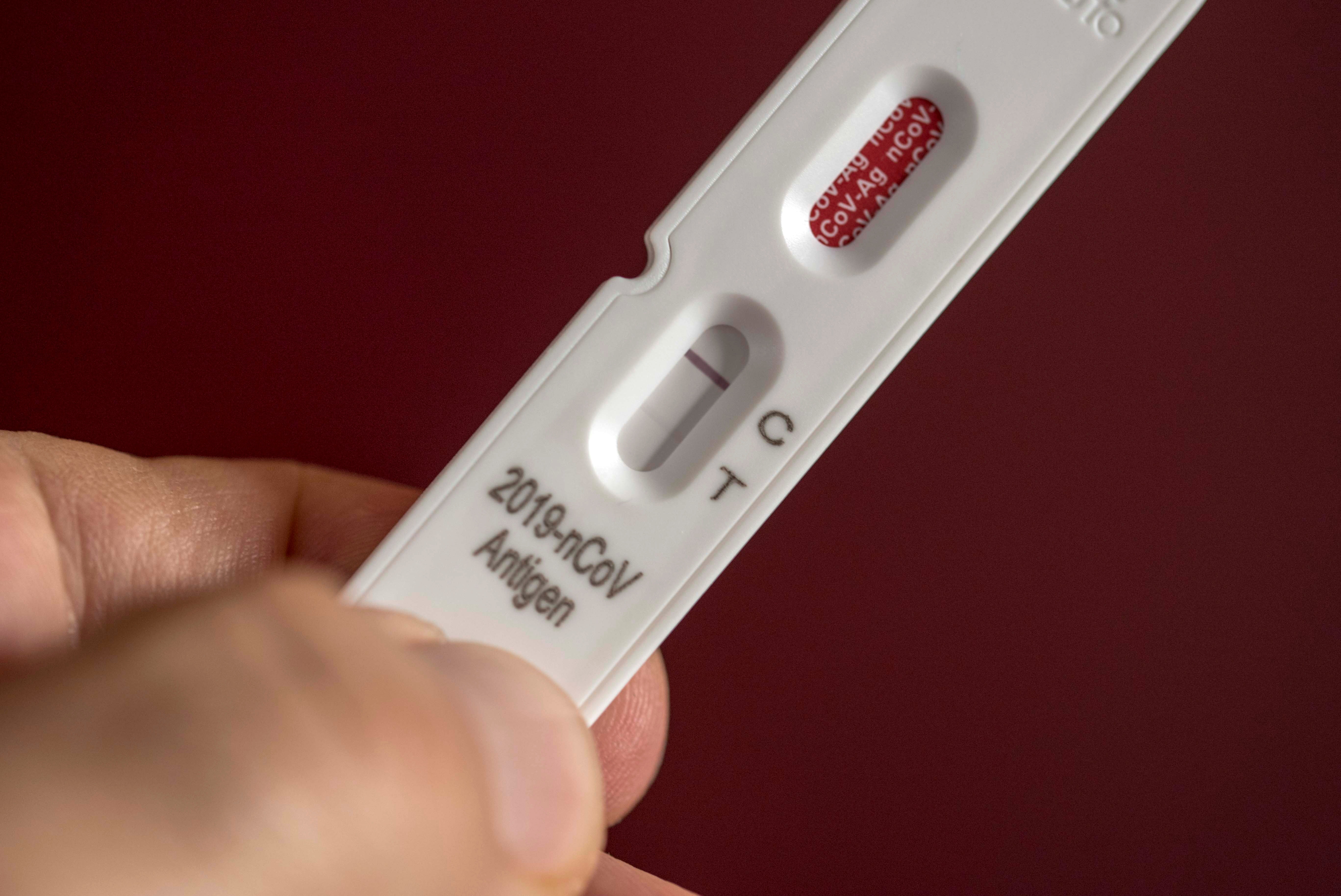
I prodotti approvati Panbio COVID-19 Antigen Self-Test, SARS-CoV-2 Antigen Self Test Nasale, SARS-CoV-2 Antigen Rapid Test (COVID-19 Ag) e WL Check SARS-CoV-2 Ag Self Testing appartengono ai laboratori Abbott, Roche, Vyam Group e Wiener e sono venduti esclusivamente in farmacia. Servono da guida diagnostica e gli utenti devono raccogliere il campione autonomamente sulla base delle istruzioni indicate dai produttori su ciascun prodotto.
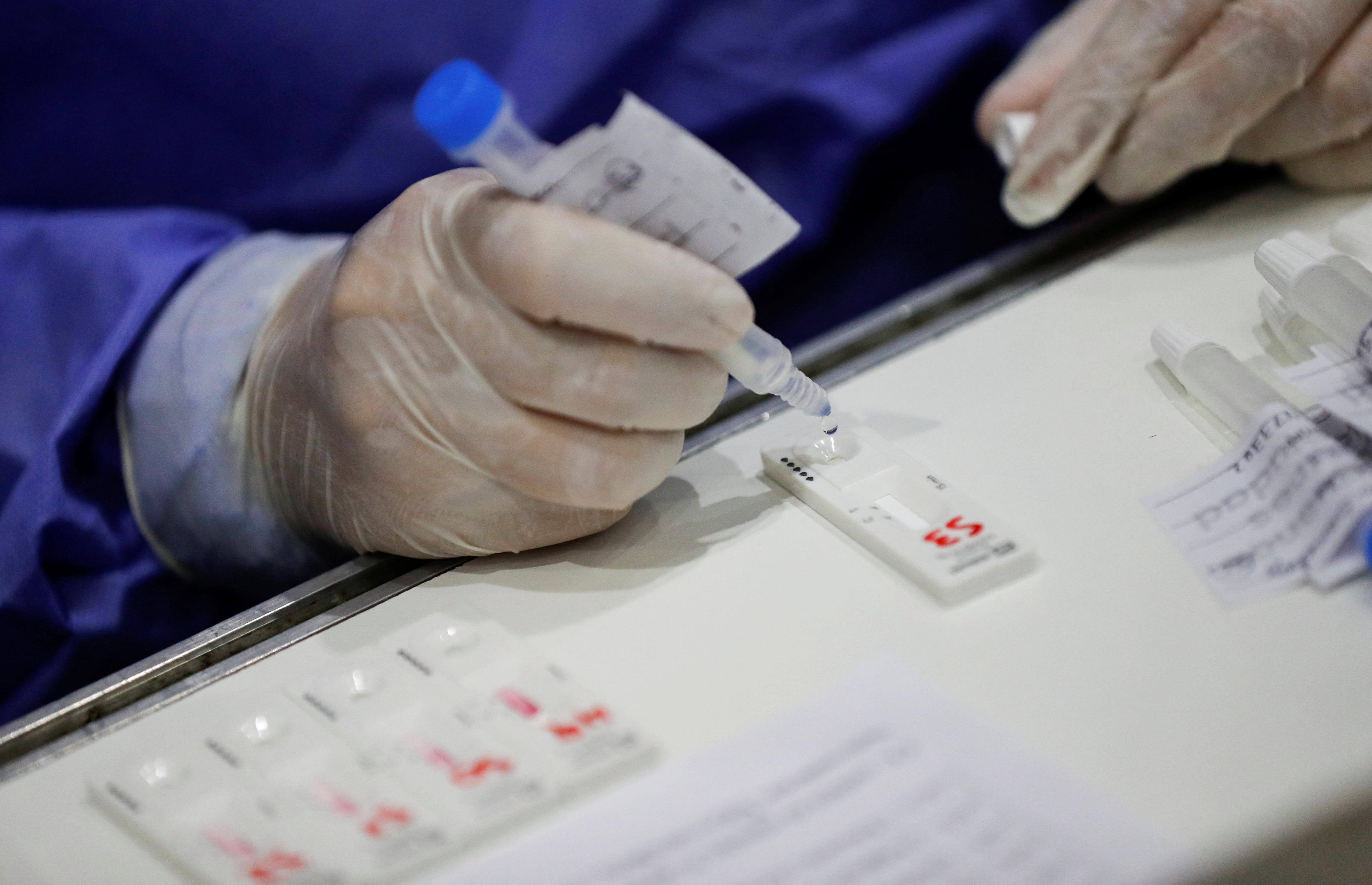
«È importante chiarire che questi test forniscono risultati indicativi, senza valore diagnostico conclusivo, tranne per il fatto che le giurisdizioni, in accordo con il Ministero della Salute della Nazione e in base alla situazione epidemiologica, considerano il risultato positivo. A differenza dei test per uso professionale in cui il campione viene prelevato a livello nasofaringeo, nel caso di test di autovalutazione viene eseguito a livello nasale o mediante saliva, come specificato dal produttore. A questo proposito, è molto importante che il campionamento venga eseguito correttamente e che il test venga eseguito immediatamente per evitare risultati errati «, ha affermato Anmat in quell'occasione.
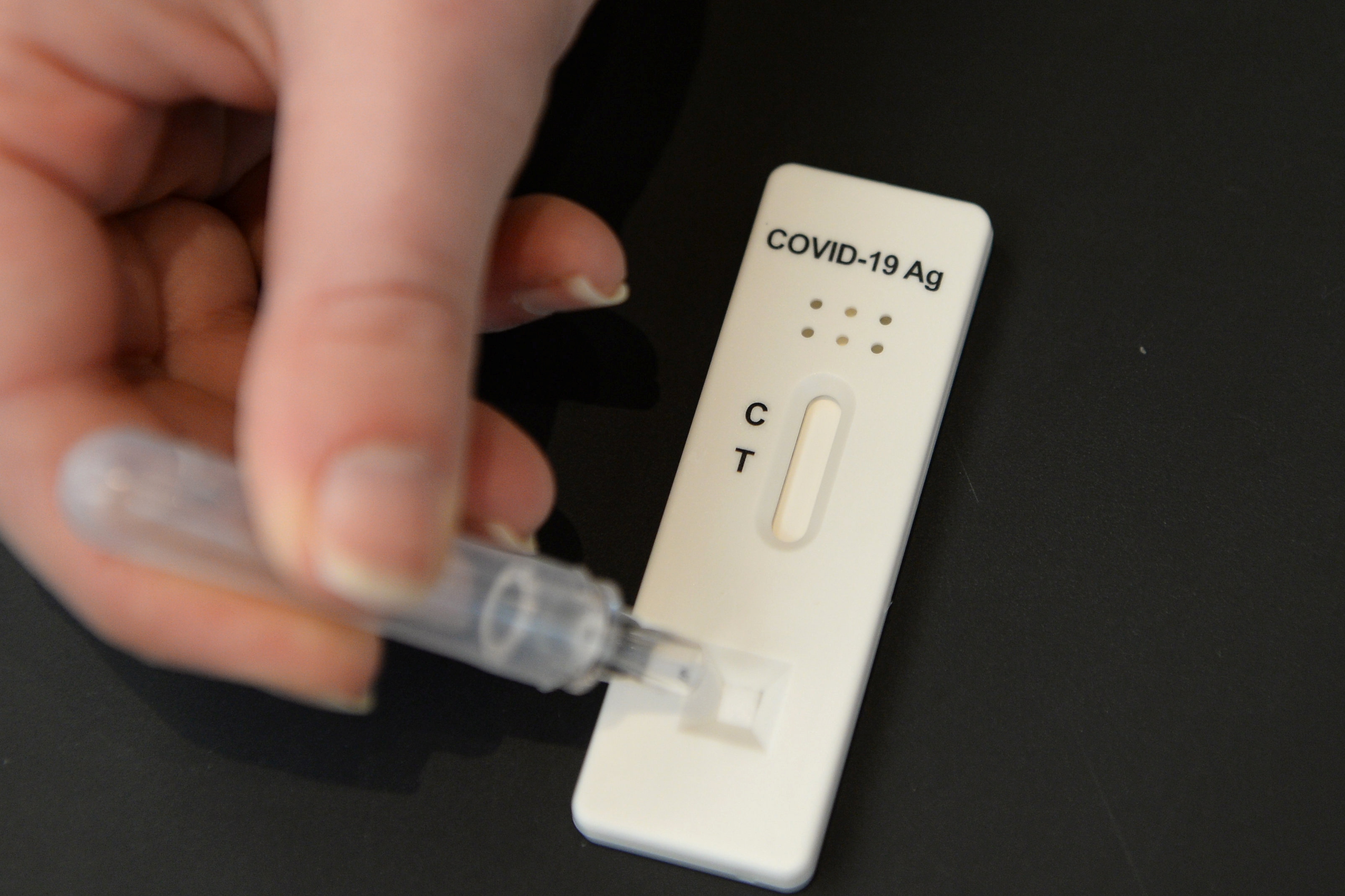
Per quanto riguarda la sua efficacia, hanno chiarito: «È necessario tenere presente che se la persona non ha sintomi o se la carica virale è bassa (che può verificarsi durante i giorni iniziali o finali dell'infezione) SARS-CoV-2 potrebbe non essere rilevata dal test, quindi un risultato negativo non esclude l'infezione. Per essere seguiti, i risultati devono essere riportati immediatamente (sulla base del codice a barre di ogni confezione) dopo che il test è stato eseguito e sarà disponibile un periodo più lungo se non è stato utilizzato, né dal singolo utente o da un funzionario segnalante in caso di un grande volume di test».
Gli esperti sottolineano che al di là del metodo scelto, ciò che deve essere preso in considerazione è il tipo di test che verrà eseguito. No, come si fa. I test effettuati con la tecnologia PCR (in particolare RT-PCR) sono più efficaci dei test antigenici, sia eseguiti con saliva che con campione nasofaringeo. Pertanto, le autorità sanitarie raccomandano di sottoporsi a un test PCR dopo essere risultato positivo per un test personale a casa per confermare se hanno COVID-19. Gli esperti considerano il test «uno strumento di salute pubblica molto utile» per fermare la diffusione della malattia. Questi test sono ampiamente utilizzati a casa, nei luoghi di lavoro e nelle scuole in gran parte del mondo.
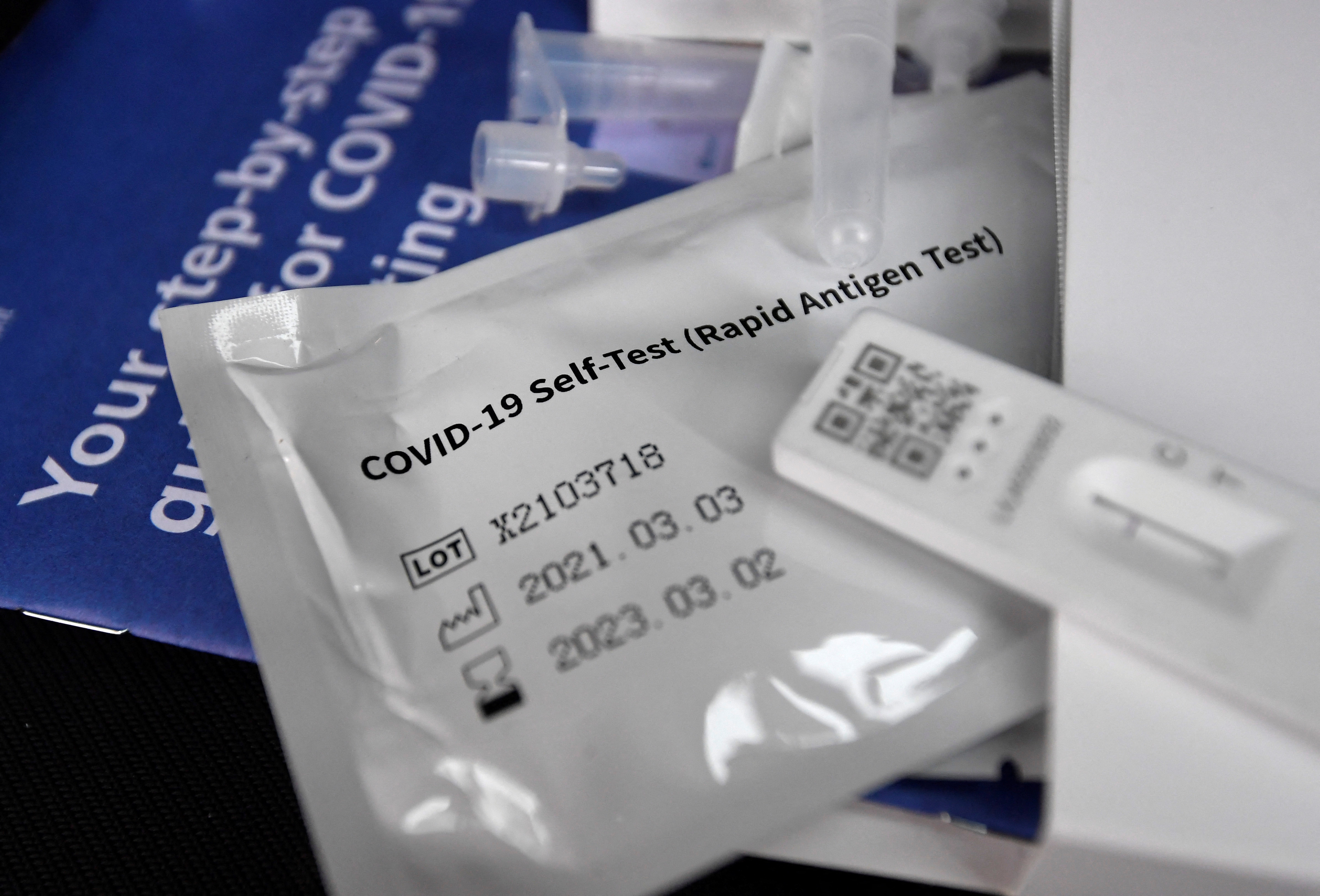
I ricercatori dell'Università di Liverpool, dell'Università di Harvard e dell'Università di Bath evidenziano in un articolo su The Lancet, che il test dell'antigene (LFT) funziona in modo molto diverso dalla polimerasi test di reazione a catena (PCR) e non possono essere confrontati.
«Il test dell'antigene non richiede strumenti o apparecchiature aggiuntivi, il che lo rende altamente portatile e può essere utilizzato in un'ampia varietà di ambienti sanitari presso i cosiddetti punti di cura e screening», ha spiegato a Infobae l'infettiologo Eduardo López (MN 37586) capo del Dipartimento di Medicina del Ricardo Gutiérrez Ospedale pediatrico.
Questo test consente grandi benefici ai reparti di emergenza, che consentirebbero la rapida identificazione dei focolai e conterrebbero la diffusione delle infezioni. Il test rapido dell'antigene rileva la proteina nucleocapsidica del virus. Questa proteina si trova sulla superficie della struttura del virus, quindi la presenza del virus si trova molto più velocemente. Da lì, il risultato è in pochi minuti. Al contrario, il test PCR cerca la presenza di materiale genetico dal virus. Tuttavia, «il test rapido non sostituisce la PCR, ma è un'ottima alternativa alla necessità di una diagnosi rapida o quando non sono disponibili diagnosi PCR», spiega López. Aggiunge: «Il Ministero della Salute riconosce questi metodi con criteri diagnostici a causa della loro elevata specificità quando sono positivi».
Gli LFT rilevano il materiale dalle proteine sulla superficie del virus e sono molto probabilmente positivi quando qualcuno è infettivo, mentre i test PCR rilevano il materiale genetico del virus, che può essere presente per settimane dopo che una persona non è più contagiosa.
L'infettiologo Ricardo Teijeiro, da parte sua, ha detto a Infobae: «Dall'inizio della pandemia c'erano diverse qualità dei test antigenici. Due anni dopo possiamo dire che gli attuali test antigenici che provengono da laboratori riconosciuti sono altamente efficaci e rispetto ai test effettuati con PCR. Ecco perché si sono dimostrati molto efficaci».
María del Mar Tomas, microbiologa dell'Ospedale A Coruña, ricercatrice presso INIBIC e portavoce di SEIMC sostiene che «la saliva è un campione molto efficace per il rilevamento della variante Ómicron se utilizziamo la tecnologia PCR (in particolare RT-PCR) o tecniche innovative come CRISPR-CAS», anche se sottolinea che i test antigenici nella saliva «sono meno efficaci e hanno una sensibilità inferiore». Omicron può essere trasmesso quando ha infettato la gola e la saliva, prima che il virus abbia raggiunto il naso, quindi passare un tampone attraverso le narici all'inizio dell'infezione non lo rileverà.
In un recente studio negli Stati Uniti, i test PCR con saliva di 29 persone infette da Omicron hanno rilevato il virus in media tre giorni prima che i campioni del naso risultassero positivi ai test dell'antigene, o cosiddetti flusso laterale. In generale, i test rapidi hanno una sensibilità inferiore rispetto ai test PCR elaborati in laboratorio, il che significa che producono più falsi negativi. Ma se il risultato è positivo, è quasi certamente il COVID-19, che rende il test antigenico un potente strumento per affrontare la pandemia.
Analisi delle varianti
I test COVID cercano piccoli frammenti del virus. Ad esempio, è comune che i test antigenici contengano anticorpi che si attaccano alle proteine o agli antigeni che si trovano sulla superficie del virus.
Ma le mutazioni del virus possono cambiare la forma di queste proteine e rendere difficile l'adesione degli anticorpi, con conseguenti falsi negativi. Così, nel gennaio 2021, i ricercatori del Center for the Development of Technologies Designed with Microsystems for Point-of-Care di Atlanta, USA, hanno iniziato a lavorare con NIH e FDA per valutare le prestazioni di decine di prodotti già autorizzati con le nuove varianti.
Gli esperimenti di laboratorio hanno inizialmente sollevato preoccupazioni sulla sensibilità di alcuni test antigenici con la variante Ómicron, ma i test sembrano funzionare meglio nel mondo reale che in laboratorio.
Dall'autunno, quando il governo di Joe Biden ha annunciato piani per fornire alle persone l'accesso ai test a casa, gli scienziati hanno anche contribuito a rendere più veloce l'autorizzazione della FDA per i prodotti che possono essere fabbricati in grandi volumi, tra cui Test sui biosensori Siemens e SD. Gli scienziati di Atlanta e il governo federale hanno creato un modello migliore e più agile: un modo sistematico per una parte indipendente di esaminare i prodotti, garantirne la qualità e accelerare l'approvazione di coloro che superano l'esame, in modo che raggiungano le mani dei consumatori più velocemente.
Questo lavoro è stato «cruciale», secondo Michael Mina, un epidemiologo di Harvard in pensione e attuale chief scientific officer di EMed, che vende test a casa. In genere, gli sviluppatori di test devono raccogliere i propri dati e seguire il processo normativo. «È un nuovo approccio che gli Stati Uniti potrebbero adottare nella valutazione degli strumenti diagnostici», ha affermato Mina.
Il programma Rapid Diagnosis (o RadX), che mira ad aiutare gli sviluppatori di test COVID a perfezionare, commercializzare e aumentare la disponibilità dei loro prodotti. Finora ha supportato 29 produttori che hanno ricevuto 40 autorizzazioni FDA per i test COVID, inclusi sette prodotti da banco; e tutti sono stati valutati dal team di Atlanta.
«Non c'è dubbio che il programma RadX abbia accelerato lo sviluppo della categoria diagnostica domestica», ha scritto Sean Parsons, CEO di Ellume, in una e-mail. «Il programma ha guidato anni di progressi nell'innovazione e nello sviluppo».
CONTINUA A LEGGERE:
Más Noticias
Para qué sirve colgar una bolsa con clavos de olor en la puerta: este es el truco casero que mezcla aroma, tradición y energía
Un creciente número de familias adopta la práctica de instalar estas especias aromáticas cerca de la entrada principal, siguiendo tradiciones que combinan creencias ancestrales y beneficios prácticos vinculados al bienestar en el ambiente doméstico. Aquí todos los trucos e información

Reconstrucción clave en el caso ‘Los Rojitos’: PNP somete a presunto sicario a diligencia científica en SJM
Junior Wilfredo Huamaní Tapia, de 28 años, fue trasladado al lugar del crimen y replicó los movimientos del agresor ante la Fiscalía

María José Pizarro criticó gobiernos anteriores y opina sobre los desafíos electorales de Iván Cepeda y el Pacto Histórico
La representante señala que el aumento de curules refleja el reconocimiento ciudadano a la labor realizada y enfatiza la necesidad de sostener la coherencia ideológica en la apuesta por el cambio político

Manifestaciones, accidentes, bloqueos en CDMX y Edomex hoy 21 de marzo:
Mantente informado en tiempo real sobre el acontecer del Valle de México

Juez fue suspendido tras declaraciones contra la Policía Nacional: “Se ha convertido en una fuerza terrorista”
Una decisión de la Comisión Nacional de Disciplina Judicial estableció que el funcionario vulneró el deber institucional al emitir opiniones generales no relacionadas con el caso tratado, lo que derivó en una sanción temporal de cuatro meses

